摘要:36.写出下列反应的化学方程式: (1)氯气与水: ; (2)二氧化碳与过氧化钠: ; (3)乙醛溶液与银氨溶液反应 .
网址:http://m.1010jiajiao.com/timu3_id_245811[举报]
二氧化硫通入氯化钡溶液中理论上不产生沉淀,而实际受到空气和溶液中氧气的影响很快便能观察到沉淀现象.为了避免产生沉淀,某化学小组设计了如下实验装置,实验操作步骤如下:

①气密性检查完好后,在装置A中的多孔隔板上放上锌粒,通过
②
③通过装置B的
④打开活塞,将产生的氢气导入后续装置一段时间.
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失.⑥拆卸装置,清洗仪器,处理剩余药品.
请回答下列问题:
(1)实验步骤①和③的空白处使用的仪器分别为
(2)装置C中苯的作用是
(3)实验步骤②的操作为
(4)实验步骤④的目的是
(5)写出实验步骤⑤试管中发生反应的化学方程式
查看习题详情和答案>>

①气密性检查完好后,在装置A中的多孔隔板上放上锌粒,通过
长颈漏斗
长颈漏斗
注入稀硫酸.打开活塞,将产生的氢气导入到后续装置.②
D中气泡均匀冒出后
D中气泡均匀冒出后
后关闭活塞,将装置D的导管插入烧杯中.③通过装置B的
分液漏斗
分液漏斗
滴加浓硫酸,产生的气体进入到BaCl2溶液中,溶液保持澄清.④打开活塞,将产生的氢气导入后续装置一段时间.
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失.⑥拆卸装置,清洗仪器,处理剩余药品.
请回答下列问题:
(1)实验步骤①和③的空白处使用的仪器分别为
长颈漏斗
长颈漏斗
、分液漏斗
分液漏斗
;(2)装置C中苯的作用是
将BaCl2溶液与空气隔离
将BaCl2溶液与空气隔离
;(3)实验步骤②的操作为
将装置D的导管口向上,用试管收集氢气验纯,待氢气纯净
将装置D的导管口向上,用试管收集氢气验纯,待氢气纯净
;(4)实验步骤④的目的是
除去SO2防止污染
除去SO2防止污染
;(5)写出实验步骤⑤试管中发生反应的化学方程式
SO2+H2O2═H2SO4、H2SO4+BaCl2═BaSO4↓+2HCl
SO2+H2O2═H2SO4、H2SO4+BaCl2═BaSO4↓+2HCl
.化学与人的身心健康密切相关.
(1)当前环境污染问题越来越严重,如酸雨、温室效应、臭氧层破坏、有毒物质的污染、汽车尾气的污染、水体污染等已成为世界各国普遍关注和研究的问题.请回答:
a、导致酸雨的主要气体是
b、使臭氧层受到破坏的主要气体是
c、为了治理汽车尾气的污染问题,可以在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成CO2和N2,写出该反应的化学方程式:
(2)合理选择饮食,正确使用药物是保证身心健康的重要方面.请回答:在日常生活中,人们在选择食物时要考虑其酸碱性.下列食物中,属于酸性食物的是
①猪肉 ②胡萝卜.
查看习题详情和答案>>
(1)当前环境污染问题越来越严重,如酸雨、温室效应、臭氧层破坏、有毒物质的污染、汽车尾气的污染、水体污染等已成为世界各国普遍关注和研究的问题.请回答:
a、导致酸雨的主要气体是
①
①
(填序号,下同).①SO2 ②CO2b、使臭氧层受到破坏的主要气体是
②
②
. ①二氧化碳②氟氯代烷c、为了治理汽车尾气的污染问题,可以在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成CO2和N2,写出该反应的化学方程式:
4CO+2NO2
4CO2+2N2
| ||
4CO+2NO2
4CO2+2N2
.
| ||
(2)合理选择饮食,正确使用药物是保证身心健康的重要方面.请回答:在日常生活中,人们在选择食物时要考虑其酸碱性.下列食物中,属于酸性食物的是
①
①
(填序号).①猪肉 ②胡萝卜.
 二氧化硫通入氯化钡溶液中理论上不产生沉淀,而实际受到空气和溶液中氧气的影响很快便能观察到沉淀现象.为了避免产生沉淀,某化学小组设计了如下实验装置,实验操作步骤如下:
二氧化硫通入氯化钡溶液中理论上不产生沉淀,而实际受到空气和溶液中氧气的影响很快便能观察到沉淀现象.为了避免产生沉淀,某化学小组设计了如下实验装置,实验操作步骤如下:①气密性检查完好后,在装置A中的多孔隔板上放上锌粒,通过
长颈漏斗
长颈漏斗
注入稀硫酸.打开活塞,将产生的氢气导入到后续装置.②
D中气泡均匀冒出后
D中气泡均匀冒出后
后关闭活塞,将装置D的导管插入烧杯中.③通过装置B的
分液漏斗
分液漏斗
滴加浓硫酸,产生的气体进入到BaCl2溶液中,溶液保持澄清.④打开活塞,将产生的氢气导入后续装置一段时间.
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失.
⑥拆卸装置,清洗仪器,处理剩余药品.
请回答下列问题
(1)实验步骤①和③的空白处使用的仪器分别为
长颈漏斗
长颈漏斗
、分液漏斗
分液漏斗
;(2)装置C中苯的作用是
将BaCl2溶液与空气隔离
将BaCl2溶液与空气隔离
;(3)实验步骤②的操作为
将装置D的导管口向上,用试管收集氢气验纯,待氢气纯净
将装置D的导管口向上,用试管收集氢气验纯,待氢气纯净
;(4)实验步骤④的目的是
除去SO2防止污染
除去SO2防止污染
;(5)写出实验步骤⑤试管中发生反应的化学方程式
SO2+H2O2=H2SO4、H2SO4+BaCl2=BaSO4↓+2HCl
SO2+H2O2=H2SO4、H2SO4+BaCl2=BaSO4↓+2HCl
;(6)为了避免产生沉淀,你认为还应采取哪些措施,请举一例
将BaCl2溶液煮沸
将BaCl2溶液煮沸
.下列A-J均是中学化学中常见物质,A、B、C、E、H是常见 气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:
气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:
试回答下列问题:
(1)I的化学式为:
(2)反应①的离子方程式:
(3)B与足量的E可生成I及另一种常见单质,写出该反应的化学方程式,并标明电子转移方向和数目:
 .
.
(4)为保证反应②的顺利进行,并得到足够量的J,应采取的措施是(写出其中两条):①
查看习题详情和答案>>
 气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:
气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:试回答下列问题:
(1)I的化学式为:
NH4Cl
NH4Cl
.(2)反应①的离子方程式:
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
.
| ||
(3)B与足量的E可生成I及另一种常见单质,写出该反应的化学方程式,并标明电子转移方向和数目:


(4)为保证反应②的顺利进行,并得到足够量的J,应采取的措施是(写出其中两条):①
氯化钠溶液必须饱和
氯化钠溶液必须饱和
②在食盐水中先通氨气至饱和再通入足量的二氧化碳气体
在食盐水中先通氨气至饱和再通入足量的二氧化碳气体
.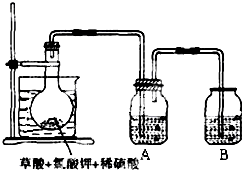 二氧化氯(ClO2)作为一种高效强氧化剂,已被联合国世界卫生组织(WHO)列为AI级安全消毒剂.常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定.温度过高,二氧化氯的水溶液有可能爆炸.某研究小组设计如图所示实验制备ClO2.
二氧化氯(ClO2)作为一种高效强氧化剂,已被联合国世界卫生组织(WHO)列为AI级安全消毒剂.常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定.温度过高,二氧化氯的水溶液有可能爆炸.某研究小组设计如图所示实验制备ClO2.(1)如图,在烧瓶中先放入一定量的KClO3和草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热.反应后产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为:
2KClO3+H2C2O4+2H2SO4
2ClO2↑+2CO2↑+2KHSO4+2H2O
| ||
2KClO3+H2C2O4+2H2SO4
2ClO2↑+2CO2↑+2KHSO4+2H2O
,
| ||
氧化产物与还原产物的物质的量之比为
1:1
1:1
.(2)控制水浴温度在60~80℃之间的目的是
使反应正常进行,并防止温度过高引起爆炸.
使反应正常进行,并防止温度过高引起爆炸.
,图示装置中缺少的一种必须的玻璃仪器是
温度计
温度计
.(3)A装置用于吸收产生的二氧化氯,其中最好盛放
②
②
.(填序号)①60℃的温水 ②冰水 ③饱和食盐水
(4)将二氧化氯溶液加入到硫化氢溶液中,所得溶液中加入少量氯化钡溶液,有白色沉淀生成.请写出二氧化氯溶液和硫化氢溶液反应的化学方程式
5H2S+8ClO2+4H2O=5H2SO4+8HCl
5H2S+8ClO2+4H2O=5H2SO4+8HCl
.