摘要:5.在2A4C-Q已达化学平衡时.能使正.逆反应速率同时加快.又使平衡向正反应方向移动.应采取的措施 [ ] A.增大压强 B.增大C的浓度 C.使用催化剂 D.升高温度
网址:http://m.1010jiajiao.com/timu3_id_243462[举报]
在2A(g)+B(g)![]() 4C(g)+D(s)+Q已达化学平衡时,能使正、逆反应速率同时加快,又使平衡向正反应方向移动,应采取的措施 ( )
4C(g)+D(s)+Q已达化学平衡时,能使正、逆反应速率同时加快,又使平衡向正反应方向移动,应采取的措施 ( )
A.增大压强 B.增大C的浓度 C.使用催化剂 D.升高温度
查看习题详情和答案>>在2A﹢B 2C﹢D反应中,表示该反应速率最快的是( )
2C﹢D反应中,表示该反应速率最快的是( )
A.v(A)=0.8mol·L-1·s-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.6mol·L-1·s-1 D.v(D)=0.5mol·L-1·s-1
在2A﹢B![]() 2C﹢D反应中,表示该反应速率最快的是( )
2C﹢D反应中,表示该反应速率最快的是( )
A.v(A)=0.8mol·L-1·s-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.6mol·L-1·s-1 D.v(D)=0.5mol·L-1·s-1
(2012?杭州一模)元素X、Y、Z、M、Q均为短周期主族元素,且原子序数依次增大.已知元素Y最高价氧化物对应水化物与它的氢化物反应能生成一种盐;Z原子最外层电子数与核外电子总数之比为3:4;M可与Z形成阴、阳离子个数比为1:2的两种化合物,Q原子的最外层电子数与次外电子数之比为3:4,YX3常温下为气体.
(1)化合物A、B由X、Z、M、Q四种元素中的三种组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为
(2)Se是人体必备的微量元素,与Q同一主族.该族二至五周期元素单质分别与H2反应生成1mol 气态氢化物的反应热如下,表示生成1mol哂化氢反应热(△H)的是
A.+99.7kJ?mol-1 B.+29.7kJ?mol-1 C.-20.6kJ?mol-1 D.-241.8kJ?mol-1
(3)X与Z、X与Q均可形成18电子分子甲和乙,写出甲、乙两种分子在水溶液中反应生成Q单质的化学方程式
(4)X、Y两种元素形成的离子化合物的电子式为
 .
.
查看习题详情和答案>>
(1)化合物A、B由X、Z、M、Q四种元素中的三种组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为
NaOH
NaOH
,B的化学式是NaHS
NaHS
.(2)Se是人体必备的微量元素,与Q同一主族.该族二至五周期元素单质分别与H2反应生成1mol 气态氢化物的反应热如下,表示生成1mol哂化氢反应热(△H)的是
B
B
(填字母代号).A.+99.7kJ?mol-1 B.+29.7kJ?mol-1 C.-20.6kJ?mol-1 D.-241.8kJ?mol-1
(3)X与Z、X与Q均可形成18电子分子甲和乙,写出甲、乙两种分子在水溶液中反应生成Q单质的化学方程式
H2O2+H2S=S+2H2O
H2O2+H2S=S+2H2O
.X和Y也可形成18电子分子丙,它通常是一种液态火箭燃料.25℃、常压下,3.2g丙在氧气中完全燃烧放出热量为62.4kJ,请写出丙完全燃烧的热化学反应方程式N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624kJ/mol
.(4)X、Y两种元素形成的离子化合物的电子式为


科学家一直致力于“人工固氮”的新方法研究.
(1)最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)?4NH3 (g)+3O2(g)+Q
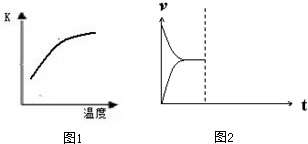
已知该反应的平衡常数K与温度的关系如图1,则此反应的 Q 0 (填“>”“<”或“=”).
(2)常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, (选填编号).
A.容器中气体的平均分子量不随时间而变化 B. v(N2)/v(O2)=2:3
C.容器中气体的密度不随时间而变化 D.通入稀有气体能提高反应的速率
(3)将反应生成的混合气体通入水中即可得氨水.用水稀释0.1mol?L-1氨水,溶液中随着水量的增加而增大的是 (填字母标号).
A.c(H+)×c(NH3?H2O)/c(OH-) B.c(NH4+)×c(OH-)/c(NH3?H2O)
C.c(H+)?c(OH-) D.
(4)常温下,在恒压密闭容器中上述反应达到平衡后,在其他条件不变时,通入2mol N2,请在图2中画出正(v正)、逆(v逆)反应速率随时间t变化的示意图.
查看习题详情和答案>>

(1)最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)?4NH3 (g)+3O2(g)+Q
已知该反应的平衡常数K与温度的关系如图1,则此反应的 Q
(2)常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,
A.容器中气体的平均分子量不随时间而变化 B. v(N2)/v(O2)=2:3
C.容器中气体的密度不随时间而变化 D.通入稀有气体能提高反应的速率
(3)将反应生成的混合气体通入水中即可得氨水.用水稀释0.1mol?L-1氨水,溶液中随着水量的增加而增大的是
A.c(H+)×c(NH3?H2O)/c(OH-) B.c(NH4+)×c(OH-)/c(NH3?H2O)
C.c(H+)?c(OH-) D.
| C(H+) | C(OH-) |
(4)常温下,在恒压密闭容器中上述反应达到平衡后,在其他条件不变时,通入2mol N2,请在图2中画出正(v正)、逆(v逆)反应速率随时间t变化的示意图.