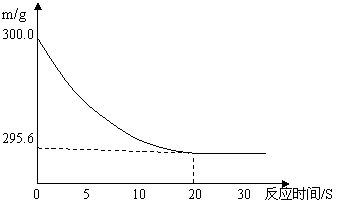
摘要:向盛有22.3 g Na2CO3和NaCl固体混合物的烧杯中加入216.1 g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量的关系如下图所示:烧杯连同药品的起始质量为300 g. 回答下列问题: (1)当固体混合物与稀盐酸恰好完全反应时.所需时间约为 S. (2)完全反应后.产生二氧化碳气体质量 g. (3)反应后.得到室温下的不饱和溶液.所得溶液中溶质的质量分数为多少? [解析]由图像变化趋势可知:从0~20秒.m逐渐减少.其原因必然是碳酸钠与盐酸反应产生二氧化碳气体跑出去了,从20秒开始.m不变了.即盐酸与碳酸钠反应结束了.故:二氧化碳的质量为300 g-295.6 g=4.4 g.然后据此代入化学方程式即可求出反应产生的碳酸钠. 答案:(1)20, (2)4.4 g, (3)解:设参加反应的碳酸钠的质量为x.反应生成的氯化钠的质量为y Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O 106 117 44 x y 4.4 解得:x=10.6 g.y=11.7 g, 烧杯里不饱和溶液中溶质总质量为: 11.7 g + = 23.4 g, 烧杯里不饱和溶液的质量为: 22.3 g+216.1 g-4.4 g = 234 g, 所得不饱和溶液的溶质质量分数:×100%=10%. 答:略. [易错点点睛]此题与例1的难度和所考知识点相似.此题的易错点是溶液质量弄错.容易把295.6 g当作溶液的质量.另外容易忽视二氧化碳的质量.
网址:http://m.1010jiajiao.com/timu3_id_24341[举报]
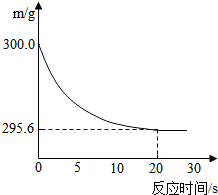 向盛有22.3 g Na2CO3和NaCl固体混合物的烧杯中加入216.1 g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示:烧杯连同药品的起始质量为300 g.回答下列问题:
向盛有22.3 g Na2CO3和NaCl固体混合物的烧杯中加入216.1 g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示:烧杯连同药品的起始质量为300 g.回答下列问题:(1)当固体混合物与稀盐酸恰好完全反应时,所需时间约为
(2)完全反应后,产生二氧化碳气体质量
(3)反应后,得到室温下的不饱和溶液.所得溶液中溶质的质量分数为多少? 查看习题详情和答案>>
向盛有22.3 g Na2CO3和NaCl固体混合物的烧杯中加入216.1g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示:烧杯连同药品的起始质量为300 g.
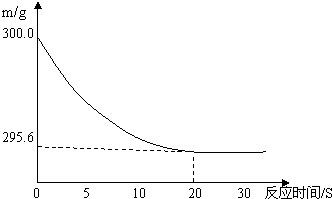
回答下列问题:
(1)当固体混合物与稀盐酸恰好完全反应时,所需时间约为 S.
(2)完全反应后,产生二氧化碳气体质量 g.
(3)反应后,得到室温下的不饱和溶液.所得溶液中溶质的质量分数为多少? 查看习题详情和答案>>

回答下列问题:
(1)当固体混合物与稀盐酸恰好完全反应时,所需时间约为
(2)完全反应后,产生二氧化碳气体质量
(3)反应后,得到室温下的不饱和溶液.所得溶液中溶质的质量分数为多少? 查看习题详情和答案>>