摘要:将0.1mol·L-1HCOONa与0.05mol·L-1HCl等体积混合后.溶液中各微粒的物质的量浓度的大小关系是 ( ) A. C(Cl-)=C=C(HCOO-)> C(H+) B.C(Cl-)> C(HCOO-)>C>C(H+) C.C(HCOO-)>C(Cl-)>C(H+)>C D.C(HCOO-)>C(Cl-)> C>C(H+)
网址:http://m.1010jiajiao.com/timu3_id_241483[举报]
(2008?唐山二模)A、B、C、D、E5瓶溶液,分别是AlCl3、BaCl2、NaHSO4、K2CO3和AgNO3中的一种.己知:
①A与B反应有气体生成. ②B与C反应有沉淀生成.
③C与D反应有沉淀生成. ④D与E反应有沉淀生成.
⑤A与E反应有气体生成. ⑥在②和③的反应中生成的沉淀是同一物质.
请填写下列空白:
(1)A是
(2)向C溶液中逐滴滴加过量稀氨水,在整个过程中出现的现象是
(3)将0.1mol/L的E溶液与O.1mol/L的Ba(OH)2溶液按下表中甲、乙、丙、丁、戊不同方式混合:
①按丁方式混合后,所得溶液显
②写出按乙方式混合时,反应的离子方程式为
③25℃时,按甲方式混合后,所得溶液的pH为
查看习题详情和答案>>
①A与B反应有气体生成. ②B与C反应有沉淀生成.
③C与D反应有沉淀生成. ④D与E反应有沉淀生成.
⑤A与E反应有气体生成. ⑥在②和③的反应中生成的沉淀是同一物质.
请填写下列空白:
(1)A是
Na2CO3
Na2CO3
,B是AlCl3
AlCl3
,D是BaCl2
BaCl2
.(2)向C溶液中逐滴滴加过量稀氨水,在整个过程中出现的现象是
先产生白色沉淀,后沉淀逐渐溶解
先产生白色沉淀,后沉淀逐渐溶解
.(3)将0.1mol/L的E溶液与O.1mol/L的Ba(OH)2溶液按下表中甲、乙、丙、丁、戊不同方式混合:
| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 0.1mol/L的Ba(OH)2溶液的体积/mL | 10 | 10 | 10 | 10 | 10 |
| 0.1mol/L的E溶液的体积/mL | 5 | 10 | 15 | 20 | 25 |
中
中
(填“酸”、“碱”或“中”)性.②写出按乙方式混合时,反应的离子方程式为
Ba2++OH-+H++SO42-═BaSO4↓+H2O
Ba2++OH-+H++SO42-═BaSO4↓+H2O
.③25℃时,按甲方式混合后,所得溶液的pH为
13
13
.按要求填空.
Ⅰ:已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
Ⅱ:(1)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因
(2)稀Na2S溶液有一种臭鸡蛋气味,加入AlCl3溶液后,臭鸡蛋气味加剧,用离子方程式表示气味加剧过程所发生的反应
III:依据氧化还原反应:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,欲采用滴定的方法测定FeSO4的质量分数,实验步骤如下:
①称量绿矾样品15.2g,配成100mL待测溶液②取10.0ml待测液置于锥形瓶中,并加入一定量的硫酸③将0.1mol?L-1的KMnO4溶液装入滴定管中,调节液面至8.00mL处④滴定待测液至滴定终点时,滴定管的液面读数18.00mL
(1)如何知道滴定到达终点?
(2)下列操作会导致测定结果偏低的是
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(3)下列每种量器的数量不限,在上述实验中,必须使用的有
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管 E容量瓶
(4)FeSO4的质量分数为
查看习题详情和答案>>
Ⅰ:已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
N2(g)+3H2(g)═2NH3(g)△H=-92kJ?mol-1
N2(g)+3H2(g)═2NH3(g)△H=-92kJ?mol-1
Ⅱ:(1)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因
Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊
Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊
如何才能用热水配制出澄清的较浓的CuSO4溶液应加入少量H2SO4
应加入少量H2SO4
;(2)稀Na2S溶液有一种臭鸡蛋气味,加入AlCl3溶液后,臭鸡蛋气味加剧,用离子方程式表示气味加剧过程所发生的反应
2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑
2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑
III:依据氧化还原反应:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,欲采用滴定的方法测定FeSO4的质量分数,实验步骤如下:
①称量绿矾样品15.2g,配成100mL待测溶液②取10.0ml待测液置于锥形瓶中,并加入一定量的硫酸③将0.1mol?L-1的KMnO4溶液装入滴定管中,调节液面至8.00mL处④滴定待测液至滴定终点时,滴定管的液面读数18.00mL
(1)如何知道滴定到达终点?
溶液由浅绿色变为紫红色,且半分钟后不变色
溶液由浅绿色变为紫红色,且半分钟后不变色
(2)下列操作会导致测定结果偏低的是
C
C
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(3)下列每种量器的数量不限,在上述实验中,必须使用的有
ABDE
ABDE
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管 E容量瓶
(4)FeSO4的质量分数为
50%
50%
.某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀.查阅资料得知常温下BaSO3的KSP为5.48×10-7,饱和亚硫酸中c(SO
)=6.3×10-8mol-1.
(1)将0.1mol?L-1的BaCl2溶液滴入饱和亚硫酸中, (填“能”或“不能”)生成BaSO3沉淀,原因是 (请写出必要的推断过程).
(2)浓硫酸的沸点为338℃,酒精灯火焰的温度为400-500℃,甲同学用装置Ⅰ进行实验,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸.
①写出加热试管中发生反应的化学方程式:
②白色沉淀的化学式是 ,请用离子方程式表示生成该白色沉淀的可能原因
(3)乙同学认为甲同学的装置不完善,设计了改进装置Ⅱ进行实验(夹持装置和A中加热装置已略,气密性已检验).
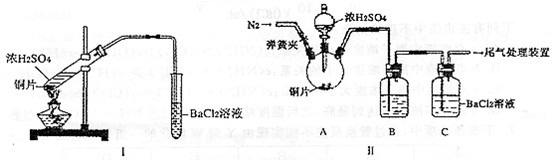
①打开弹簧夹,通入N2一段时间后关闭弹簧夹
②滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成.操作①的目的是 ,洗气瓶B中的试剂是 .
(4)丙同学取乙实验后的C中溶液少许,滴加一种无色溶液,也产生不溶于盐酸的白色沉淀,丙滴加的试剂可能是 .
A.NaOH 溶液 B.Na[Al(OH)4]溶液 C.H2O2 溶液 D.酸性 KMnO4 溶液.
查看习题详情和答案>>
2- 3 |
(1)将0.1mol?L-1的BaCl2溶液滴入饱和亚硫酸中,
(2)浓硫酸的沸点为338℃,酒精灯火焰的温度为400-500℃,甲同学用装置Ⅰ进行实验,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸.
①写出加热试管中发生反应的化学方程式:
②白色沉淀的化学式是
(3)乙同学认为甲同学的装置不完善,设计了改进装置Ⅱ进行实验(夹持装置和A中加热装置已略,气密性已检验).

①打开弹簧夹,通入N2一段时间后关闭弹簧夹
②滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成.操作①的目的是
(4)丙同学取乙实验后的C中溶液少许,滴加一种无色溶液,也产生不溶于盐酸的白色沉淀,丙滴加的试剂可能是
A.NaOH 溶液 B.Na[Al(OH)4]溶液 C.H2O2 溶液 D.酸性 KMnO4 溶液.