摘要: a.c 3 Cu(OH)2
网址:http://m.1010jiajiao.com/timu3_id_241367[举报]
Ⅰ.现在四种化学仪器:A.量筒 B.容量瓶 C.滴定管 D.烧杯
(1)标有“0”刻度的化学仪器为 ;(填代号,下同)
(2)实验时,要用所装液体润洗的是 ;
(3)使用前要检验是否漏水的仪器 ;
(4)量取液体体积时,平视时读数为n mL,仰视时读数为x mL,俯视时读数为y mL,若x<n<y,则所用的仪器为 .
Ⅱ.某实验小组欲从硫酸铜和硫酸亚铁的酸性混合溶液中分离出硫酸亚铁溶液,经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH值如下表:
实验室有下列试剂可供选择:H2O2、CaO、CuO、稀H2SO4、铁粉
(1)分离实验的实验操作步骤和目的为:
(2)步骤4中需要的玻璃仪器为 、 、 ;检验沉淀洗涤干净的操作方法为 .
查看习题详情和答案>>
(1)标有“0”刻度的化学仪器为
(2)实验时,要用所装液体润洗的是
(3)使用前要检验是否漏水的仪器
(4)量取液体体积时,平视时读数为n mL,仰视时读数为x mL,俯视时读数为y mL,若x<n<y,则所用的仪器为
Ⅱ.某实验小组欲从硫酸铜和硫酸亚铁的酸性混合溶液中分离出硫酸亚铁溶液,经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH值如下表:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
(1)分离实验的实验操作步骤和目的为:
| 实验步骤 | 实验操作 | 实验操作目的 |
| 步骤1 | ||
| 步骤2 | ||
| 步骤3 | ||
| 步骤4 | 洗涤沉淀 | |
| 步骤5 | 得到FeSO4溶液 |
Ⅰ.现在四种化学仪器:A.量筒 B.容量瓶 C.滴定管 D.烧杯
(1)标有“0”刻度的化学仪器为 ;(填代号 ,下同)[来源:学+科+网]
(2)实验时,要用所装液体润洗的是 ;
(3)使用前要检验是否漏水的仪器 ;
(4) 量取液体体积时,平视时读数为n mL,仰视时读数为x mL,俯视时读数为y mL,若x<n<y,则所用的仪器为 。
Ⅱ.某实验小组欲从硫酸铜和硫酸亚铁的酸性混合溶液中分离出硫酸亚铁溶液,经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH值如下表:
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀pH |
6.0 |
7.5 |
1.4 |
|
沉淀完全pH |
13 |
14 |
3.7 |
实验室有下列试剂可供选择:H2O2、CaO、CuO、稀H2SO4、铁粉
(1)分离实验的实验操作步骤和目的为:
|
实验步骤 |
实验操作 |
实验操作目的 |
|
步骤1 |
|
|
|
步骤2 |
|
|
|
步骤3 |
|
|
|
步骤4 |
洗涤沉淀 |
[来源:] |
|
步骤5 |
|
得到FeSO4溶液 |
(2)步骤4中需要的玻璃仪器为 、 、 ;检验沉淀洗涤干净的操作方法为 。
查看习题详情和答案>>
研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+l价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2,CO等还原,也能被氮的气态氢化物还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、______(填字母).A.AlCl3溶液B.NaOH溶液 C.稀H2SO4 D.H2O4溶液 假若Cu(OH)2具有两性,应该看到的实验现象是______.
(2)为了比较Cu+l价化合物和+2价化合物的稳定性,他们取Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末氧化亚铜.向氧化亚铜中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.可以得出的结论是______.根据以上现象写出氧化亚铜和稀硫酸反应的离子方程式______.
(3)为解决问题③,设计了如下的实验装置(夹持装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体Y.现有氮的某种气态氢化物X气体0.0lmol,缓缓通过红热的氧化铜玻璃管完全反应后,测得C装置增重0.36g并收集到单质气体Y0.28g.X气体的摩尔质量______,B中发生反应的化学方程式为______.
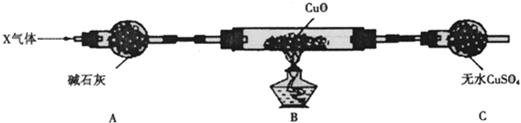
(4)请猜测用上述装置测量时有可能产生误差的原因______(答1条即可)
查看习题详情和答案>>
研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+l价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2,CO等还原,也能被氮的气态氢化物还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、 (填字母).A.AlCl3溶液B.NaOH溶液 C.稀H2SO4 D.H2O4溶液 假若Cu(OH)2具有两性,应该看到的实验现象是 .
(2)为了比较Cu+l价化合物和+2价化合物的稳定性,他们取Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末氧化亚铜.向氧化亚铜中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.可以得出的结论是 .根据以上现象写出氧化亚铜和稀硫酸反应的离子方程式 .
(3)为解决问题③,设计了如下的实验装置(夹持装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体Y.现有氮的某种气态氢化物X气体0.0lmol,缓缓通过红热的氧化铜玻璃管完全反应后,测得C装置增重0.36g并收集到单质气体Y0.28g.X气体的摩尔质量 ,B中发生反应的化学方程式为 .
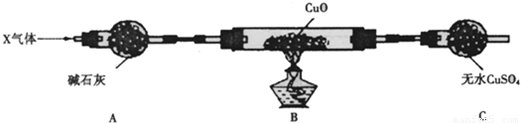
(4)请猜测用上述装置测量时有可能产生误差的原因 (答1条即可) 查看习题详情和答案>>
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+l价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2,CO等还原,也能被氮的气态氢化物还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、 (填字母).A.AlCl3溶液B.NaOH溶液 C.稀H2SO4 D.H2O4溶液 假若Cu(OH)2具有两性,应该看到的实验现象是 .
(2)为了比较Cu+l价化合物和+2价化合物的稳定性,他们取Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末氧化亚铜.向氧化亚铜中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.可以得出的结论是 .根据以上现象写出氧化亚铜和稀硫酸反应的离子方程式 .
(3)为解决问题③,设计了如下的实验装置(夹持装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体Y.现有氮的某种气态氢化物X气体0.0lmol,缓缓通过红热的氧化铜玻璃管完全反应后,测得C装置增重0.36g并收集到单质气体Y0.28g.X气体的摩尔质量 ,B中发生反应的化学方程式为 .

(4)请猜测用上述装置测量时有可能产生误差的原因 (答1条即可) 查看习题详情和答案>>
根据下列流程处理废旧电路板来回收金属Cu,并制得高铁酸钾(K2FeO4).据此回答问题:

(1)试剂a为 ,试剂b为 (填写所选试剂代号)
A.浓硫酸 B.硫酸铁溶液 C.氯水 D.H2O2和稀硫酸 E.Fe
(2)加入过量试剂c,发生反应的离子方程式为 ;溶液Z中金属离子可能有Cu2+、Fe2+、Fe3+,检验Fe3+的试剂为 (填化学式);欲测定溶液Z中Fe2+的浓度,需要用(填仪器名称) 配制一定浓度的KMnO4标准溶液.在滴定时KMnO4标准溶液应加入到 (填“酸式”或“碱式”)滴定管中.
(3)K2FeO4是强氧化剂,与水发生反应:4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-,产生11.2L(标况)O2时,转移电子的物质的量为 .K2FeO4与FeCl3相比,净水效果更好的是 ,理由是 .
(4)高铁电池是一种新型可充电电池,总反应为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH,该电池放电时正极反应式是: .
查看习题详情和答案>>

(1)试剂a为
A.浓硫酸 B.硫酸铁溶液 C.氯水 D.H2O2和稀硫酸 E.Fe
(2)加入过量试剂c,发生反应的离子方程式为
(3)K2FeO4是强氧化剂,与水发生反应:4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-,产生11.2L(标况)O2时,转移电子的物质的量为
(4)高铁电池是一种新型可充电电池,总反应为:3Zn+2K2FeO4+8H2O
| 放电 | 充电 |