摘要:17.为了将混有硫酸钠的氯化钠提纯.并制得纯净的氯化钠溶液.某学生设计如下实验: (1)操作①能否用硝酸钡溶液?说明理由 . (2)进行操作①后.如何判断SO已除尽.方法是 . (3)操作②的目的是 .为什么不先过滤而后加碳酸钠溶液.其理由是 . [答案](1)不能.会引入新的杂质(NO) (2)取少量上层澄清溶液.滴加BaCl2溶液.如无沉淀出现.说明SO除尽 (3)除去过量的Ba2+ 一次性过滤出BaSO4和BaCO3沉淀
网址:http://m.1010jiajiao.com/timu3_id_239385[举报]
为了将混有硫酸钠的氯化钠提纯,并制得纯净的氯化钠溶液,某学生设计如下实验:
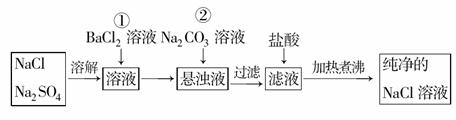
(1)操作①能否用硝酸钡溶液?说明理由__________________。
(2)进行操作①后,如何判断SO![]() 已除尽,方法是_____________ ________________。
已除尽,方法是_____________ ________________。
(3)操作②的目的是__________________,为什么不先过滤而后加碳酸钠溶液,其理由是__________________________。
查看习题详情和答案>>为了将混有硫酸钠、氯化铵的氯化钠固体提纯,并制得纯净的氯化钠溶液,某学生设计了图所示实验.根据图回答下列问题.

(1)操作①发生反应的化学方程式为
(2)操作②中能否用硝酸钡溶液?
(3)进行操作②后,判断SO42-已经除尽的方法是
(4)操作④需要用到的玻璃仪器是
(5)此实验最终并不能得到纯净的NaCl溶液,改进的方法是
查看习题详情和答案>>

(1)操作①发生反应的化学方程式为
NH4Cl
NH3↑+HCl↑
| ||
NH4Cl
NH3↑+HCl↑
.
| ||
(2)操作②中能否用硝酸钡溶液?
否
否
(填写“能”或“否”).说明理由用硝酸钡会引入新杂质NO3-
用硝酸钡会引入新杂质NO3-
.(3)进行操作②后,判断SO42-已经除尽的方法是
取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42-已除尽,反之则有(或其他的方法)
取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42-已除尽,反之则有(或其他的方法)
.(4)操作④需要用到的玻璃仪器是
玻璃棒、漏斗、烧杯
玻璃棒、漏斗、烧杯
.(5)此实验最终并不能得到纯净的NaCl溶液,改进的方法是
在⑤处应先加入过量的盐酸后再加热煮沸
在⑤处应先加入过量的盐酸后再加热煮沸
.为了将混有硫酸钠、碳酸氢铵的氯化钠提纯,并制得纯净的氯化钠溶液,某学生设计如图所示实验.
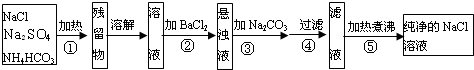
(1)操作②能否用硝酸钡溶液?说明理由.______
(2)进行操作②后,如何判断SO42-已除尽,方法是______
(3)操作③目的是______;
④步操作需要用到的玻璃仪器有哪些______.
(4)此方案是否严密,说明理由______.
查看习题详情和答案>>

(1)操作②能否用硝酸钡溶液?说明理由.______
(2)进行操作②后,如何判断SO42-已除尽,方法是______
(3)操作③目的是______;
④步操作需要用到的玻璃仪器有哪些______.
(4)此方案是否严密,说明理由______.
为了将混有硫酸钠、碳酸氢铵的氯化钠提纯,并制得纯净的氯化钠溶液,某学生设计如下实验:

(1)操作②能否用硝酸钡溶液?____。理由是____。
(2)进行操作②后,如何判断SO42-已除尽,方法是____。
(3)操作③的目的是_____;为什么不先过滤而后加碳酸钠溶液,其理由是____。
(4)此设计方案是否严密,如不严密,说明如何改进_____________。
查看习题详情和答案>>
(2)进行操作②后,如何判断SO42-已除尽,方法是____。
(3)操作③的目的是_____;为什么不先过滤而后加碳酸钠溶液,其理由是____。
(4)此设计方案是否严密,如不严密,说明如何改进_____________。
为了将混有硫酸钠、碳酸氢铵的氯化钠提纯,并制得纯净的氯化钠溶液,某学生设计如下实验:

(1)操作②能否用硝酸钡溶液?说明理由________________________________________。
(2)进行操作②后,如何判断![]() 已除尽,方法是_________________________________。
已除尽,方法是_________________________________。
(3)操作③的目的是_________________________________;为什么不先过滤而后加碳酸钠溶液,其理由是_________________________________________________________。
(4)此设计方案是否严密,说明理由_________________________________________________。
查看习题详情和答案>>