摘要:(1)C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O (2)无水CuSO4.验证产物中有水蒸汽, 品红溶液.验证产物中有SO2, 澄清石灰水.验证产物中有CO2 (3)紫色未全部褪去
网址:http://m.1010jiajiao.com/timu3_id_236461[举报]
下列各反应中使用的硫酸是稀H2SO4的是
- A.3Zn+4H2SO4=3ZnSO4+S↓+4H2O
- B.2Ag+2H2SO4=Ag2SO4+SO2↑+2H2O
- C.C+2H2SO4=CO2↑+2SO2↑+2H2O
- D.Zn+H2SO4=ZnSO4+H2↑
中学常见反应的化学方程式是A+B----->X+Y+H2O(未配平,反应条件略去),其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,则Y的化学式是
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为浓硫酸,则化学方程式为:
(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中.A元素为
查看习题详情和答案>>
(1)若Y是黄绿色气体,则Y的化学式是
Cl2
Cl2
.(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为浓硫酸,则化学方程式为:
C+2H2SO4
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4
CO2↑+2SO2↑+2H2O
,则反应中氧化剂与还原剂的物质的量之比是
| ||
2:1
2:1
.(3)若A为金属单质,常温下A在B的浓溶液中发生“钝化”,且A为短周期元素,且A可溶于NaOH溶液中.A元素为
Al
Al
(填化学式),其所在周期表中的位置为:第三周期,ⅢA族
第三周期,ⅢA族
(填所在周期和族);A与NaOH反应的离子方程式是2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.如图是木炭与浓硫酸反应并检验反应产物的装置图,根据所学知识回答相关问题
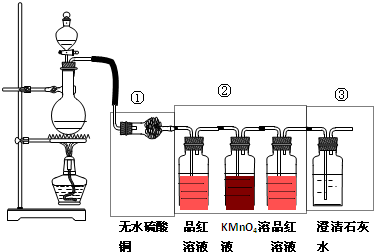
(1)写出烧瓶中发生反应的化学方程式:
(2)无水硫酸铜的现象是
(3)第一个洗气瓶中的品红溶液
(4)KMnO4的作用是
(5)第二个洗气瓶中的品红溶液的作用是
(6)澄清石灰水的现象是
查看习题详情和答案>>

(1)写出烧瓶中发生反应的化学方程式:
C+2H2SO4
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4
CO2↑+2SO2↑+2H2O
;
| ||
(2)无水硫酸铜的现象是
变蓝色
变蓝色
,用以检验水
水
的生成;(3)第一个洗气瓶中的品红溶液
褪色
褪色
,说明生成了生成SO2
生成SO2
;(4)KMnO4的作用是
除去SO2
除去SO2
,现象是褪色
褪色
;(5)第二个洗气瓶中的品红溶液的作用是
检验S02是否完全除尽
检验S02是否完全除尽
;(6)澄清石灰水的现象是
变浑
变浑
,反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
.