网址:http://m.1010jiajiao.com/timu3_id_235614[举报]
我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库。目前,世界各国都在研究如何充分利用海洋资源。
(1)全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg·L-1。其工业提取法有:
Ⅰ、空气吹出纯碱吸收法。方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴。该方法涉及的反应有:
①_________________(写出离子方程式);
②3Br2+3CO32-=BrO3-+5Br-+3CO2↑;
③_________________(写出离子方程式)。
其中反应②中氧化剂是_________,还原剂是___________
Ⅱ、空气吹出SO2吸收法。该方法基本同⑴,只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴。
写出溴与二氧化硫反应的化学方程式 ____________________ 。
Ⅲ、溶剂萃取法。该法是利用单质溴在水中和萃取剂中溶解度的不同的原理来进行的。
实验室中萃取用到的实验仪器名称是 ___________________。
下列可以用于海水中溴的萃取的试剂是 __________。①乙醇,②四氯化碳,③硝酸
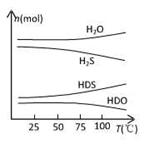
 (2)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。
(2)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。
右图为“硫化氢-水双温交换法”所发生的两个
反应中涉及的四种物质在反应体系中的物质的量随温
度的变化曲线。写出100℃时所发生的反应的化学方
程式________________________________________;
工业上富集HDO的生产过程中,可以循环利用的一种
物质是____________________。
查看习题详情和答案>>我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库。目前,世界各国都在研究如何充分利用海洋资源。
(1)全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg·L-1。其工业提取法有:
Ⅰ、空气吹出纯碱吸收法。方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴。该方法涉及的反应有:
①_________________(写出离子方程式);
②3Br2+3CO32-=BrO3-+5Br-+3CO2↑;
③_________________(写出离子方程式)。
其中反应②中氧化剂是_________,还原剂是___________
Ⅱ、空气吹出SO2吸收法。该方法基本同⑴,只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴。
写出溴与二氧化硫反应的化学方程式 ____________________ 。
Ⅲ、溶剂萃取法。该法是利用单质溴在水中和萃取剂中溶解度的不同的原理来进行的。
实验室中萃取用到的实验仪器名称是 _________________。
下列可以用于海水中溴的萃取的试剂是 __________。①乙醇,②四氯化碳,③硝酸
(2)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO。其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO。
右图为“硫化氢-水双温交换法”所发生的两个反应中涉及的四种物质在反应体系中的物质的量随温度的变化曲线。写出100℃时所发生的反应的化学方程式________________________________________;工业上富集HDO的生产过程中,可以循环利用的一种物质是____________________。
电解原理在化学工业中有广泛应用。右下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
 (1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,
同时在两边各滴入几滴酚酞试液,则可观察到
在X极附近观察到的现象是
电极反应式是
检验Y电极反应产物的方法是
电极反应式是 、发生 反应
电解一段时间之后溶液的PH将会 (升高、降低或不变)
总方程式为
(2)若X、Y都是铜电极,a是稀CuSO4溶液,开始实验,X极的电极反应式是 。
Y电极的电极反应式是 ,电解前后CuSO4溶液的浓度 (变大、变小或不变)若X电极质量增重64克,则在电路中有 mol的电子发生转移。
查看习题详情和答案>> 生物质资源是一种污染小的可再生能源.生物质的主要转化途径及主要产物如图.
生物质资源是一种污染小的可再生能源.生物质的主要转化途径及主要产物如图.(1)由生物质能获得的CO和H2,可以合成甲醇和二甲醚(CH3OCH3)及许多烃类物质.当两者1:1催化反应,其原子利用率达100%,合成的物质可能是
a.汽油 b.甲醇 c.甲醛 d.乙酸
(2)甲醇是一种重要的化工原料,工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ?mol-1.
若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | α 1 | α 2 | α 3 |
a.c1=c2 b.2Q1=Q3 c.K1=K3 d.α2+α3<100%
(3)在一定温度和压强下,CO和H2催化合成二甲醚的反应为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)

①若一体积可变的密闭容器中充入3mol H2、3mol CO、1mol CH3OCH3、1mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍.则:反应开始时:v(正)>v(逆)的理由是:
平衡时,n(CH3OCH3)=
②右图为绿色电源“二甲醚燃料电池”的工作原理示意图.b电极是