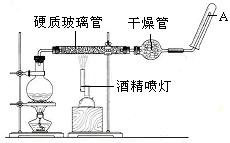
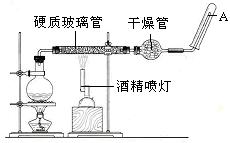
摘要:23.在常温下.Fe与水并不起反应.但在高温下.Fe与水蒸气可发生反应. 应用下列装置.在硬质玻璃管中放入还原铁粉和石棉绒的混合物.加热.并通入水蒸气.就可以完成高温下“Fe与水蒸气的反应实验 . 请回答该实验中的问题. (1)写出该反应的化学方程式 .其中氧化剂是 .还原剂是 .8.4g铁粉参加反应.转移电子 mol. (2)玻璃管中石棉绒的作用是 .实验开始时应先点燃 .实验结束时应先熄灭 . (3)圆底烧瓶中盛装的水.该装置受热后的主要作用是 ,烧瓶里应事先放置 .其作用是 . (4)该同学欲确定反应后硬质试管中固体物质的成分.设计了如下实验方案: ①待硬质试管冷却后.取少许其中的固体物质溶于稀硫酸得溶液B, ②取少量溶液B滴加KSCN溶液.若溶液变红色则说明硬质试管中固体物质的 成分是 .若溶液未变红色则说明硬质试管中固体物质的 成分是 . (5)该同学按上述实验方案进行了实验.结果溶液未变红色.原因是 . (6)该同学马上另取少量溶液B.使其跟NaOH溶液反应. 若按右图所示的操作.可观察到生成白色沉淀.迅速变成 灰绿色.最后变成红褐色的现象.请写出与上述现象相关 的反应的化学方程式 . . (7)一段时间后.该同学发现(4)中未变红的溶液变成红色.说明Fe2+ 具有 性.由此可知.实验室中含Fe2+的盐溶液现用现配制的原因是 . 并且配制含Fe2+的盐溶液时应加入少量 . 梅州市曾宪梓中学2010-2011学年度第一学期期末考试试卷
网址:http://m.1010jiajiao.com/timu3_id_232318[举报]
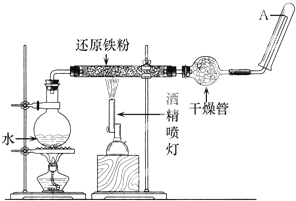 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.请回答该实验中的问题.
(1)写出该反应的化学方程式
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
.
| ||
(2)实验前必须对整套装置进行的操作是
检验装置的气密性
检验装置的气密性
.(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是
为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气
为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气
.(4)试管中要收集干燥的气体,干燥管中盛装的物质是
碱石灰
碱石灰
,作用是除去反应产生的H2中的水蒸气
除去反应产生的H2中的水蒸气
.(5)试管中收集到的气体是
氢气
氢气
,如果要在A处玻璃管口处点燃该气体,则必须对该气体进行验纯
验纯
,这一操作的目的是防止点燃时,氢气因含有氧气而爆炸
防止点燃时,氢气因含有氧气而爆炸
.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 请回答该实验中的问题.

(1)写出该反应的化学方程式
(2)玻璃管中石棉绒的作用是
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是
查看习题详情和答案>>

(1)写出该反应的化学方程式
3Fe+4H2O(g)
Fe 3O4+4 H2
| ||
3Fe+4H2O(g)
Fe 3O4+4 H2
,其中氧化剂是
| ||
H2O
H2O
,还原剂是Fe
Fe
.8.4g铁粉参加反应,转移电子0.4
0.4
mol.(2)玻璃管中石棉绒的作用是
铁粉的载体,增大铁粉与水蒸气的接触面
铁粉的载体,增大铁粉与水蒸气的接触面
,实验开始时应先点燃酒精灯
酒精灯
,实验结束时应先熄灭酒精喷灯
酒精喷灯
.(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是
为实验提供水蒸气
为实验提供水蒸气
;烧瓶底部应事先放置碎瓷片
碎瓷片
,其作用是防止暴沸
防止暴沸
. 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.(1)写出该反应的反应方程式:
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
| ||
(2)实验前必须进行的操作是
检验装置的气密性
检验装置的气密性
.(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是
为实验提供水蒸气
为实验提供水蒸气
;(4)酒精灯和酒精喷灯点燃的顺序是
先点燃酒精灯,后点燃酒精喷灯
先点燃酒精灯,后点燃酒精喷灯
.(5)干燥管中盛装是的物质是
碱石灰
碱石灰
.(6)如果要在A处玻璃管处点燃该气体,则必须对该气体进行
验纯
验纯
.