题目内容
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 请回答该实验中的问题.

(1)写出该反应的化学方程式
(2)玻璃管中石棉绒的作用是
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是

(1)写出该反应的化学方程式
3Fe+4H2O(g)
Fe 3O4+4 H2
| ||
3Fe+4H2O(g)
Fe 3O4+4 H2
,其中氧化剂是
| ||
H2O
H2O
,还原剂是Fe
Fe
.8.4g铁粉参加反应,转移电子0.4
0.4
mol.(2)玻璃管中石棉绒的作用是
铁粉的载体,增大铁粉与水蒸气的接触面
铁粉的载体,增大铁粉与水蒸气的接触面
,实验开始时应先点燃酒精灯
酒精灯
,实验结束时应先熄灭酒精喷灯
酒精喷灯
.(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是
为实验提供水蒸气
为实验提供水蒸气
;烧瓶底部应事先放置碎瓷片
碎瓷片
,其作用是防止暴沸
防止暴沸
.分析:(1)对于铁与水蒸气反应的化学方程式,教材中已出现,很容易写出化学方程式.还原剂的判定方法根据化合价升高的物质,氧化剂是化合价降低的物质;根据3Fe+4H2O(g)
Fe 3O4+4 H2;方程式中反应3mol铁原子转移8个电子.
(2)增大铁粉与水蒸气的接触面;如果在一套装置中需要两处加热,一定要注意点燃加热仪器的顺序,一般是根据实验的安全性和对实验结果的影响来考虑;
(3)反应物为水蒸气与铁;放碎瓷片的目的是防止沸腾事故发生;
| ||
(2)增大铁粉与水蒸气的接触面;如果在一套装置中需要两处加热,一定要注意点燃加热仪器的顺序,一般是根据实验的安全性和对实验结果的影响来考虑;
(3)反应物为水蒸气与铁;放碎瓷片的目的是防止沸腾事故发生;
解答:解:(1)铁与水蒸气发生氧化还原反应:3Fe+4H2O
Fe3O4+4H2,根据化合价升降来判断氧化剂和还原剂.因铁的化合价升高,所以铁作还原剂,水中氢的化合价降低,水作氧化剂;根据3Fe+4H2O(g)
Fe 3O4+4 H2;方程式中反应3mol铁原子转移8个电子,设转移电子物质的量为X,
3Fe≈8e-
3×56 8
8.4g x
=
解得:x=0.4mol,
故答案为:3Fe+4H2O(g)
Fe 3O4+4H2;H2O;Fe;0.4;
(2)增大铁粉与水蒸气的接触面;点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,
故答案为:铁粉的载体,增大铁粉与水蒸气的接触面;酒精灯;酒精喷灯;
(3)因为反应物为水蒸气与铁,所以这里加热的目的就是提供水蒸气,烧瓶底部应事先放置碎瓷片,放碎瓷片的目的是防止沸腾事故发生,
故答案为:为实验提供水蒸气;碎瓷片;防止暴沸.
| ||
| ||
3Fe≈8e-
3×56 8
8.4g x
| 3×56 |
| 8.4g |
| 8 |
| x |
解得:x=0.4mol,
故答案为:3Fe+4H2O(g)
| ||
(2)增大铁粉与水蒸气的接触面;点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,
故答案为:铁粉的载体,增大铁粉与水蒸气的接触面;酒精灯;酒精喷灯;
(3)因为反应物为水蒸气与铁,所以这里加热的目的就是提供水蒸气,烧瓶底部应事先放置碎瓷片,放碎瓷片的目的是防止沸腾事故发生,
故答案为:为实验提供水蒸气;碎瓷片;防止暴沸.
点评:本题考查铁及其化合物的性质实验,难度不大,电子数计算是本题的难点.

练习册系列答案
相关题目
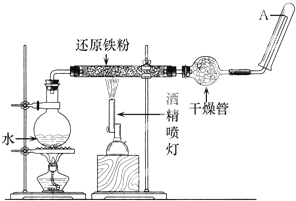 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“. 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.