摘要:澄清的石灰水变浑浊 白色固体变蓝 2 CuO + H2O CuCO3 CuO + CO2 ↑ (8)4CuO 2Cu2O + O2 ↑ 3.34.某校兴趣小组的同学在网上看到:茶叶是碱性食品.喝茶可以溶浴解脂肪而减肥.他们设计了探究的课题是:比较不同产地茶叶泡出液的酸碱度及茶水是否能溶解脂肪而有减肥作用.他们的实验过程如塑下: ①从市场上购买了三种不同产地的茶叶.编号为A.B.C. ②取A.B.C三种茶叶分别在相同的条件下.用开水冲泡. ③用pH试纸分别到杯中蘸取A.B.C三种茶叶的泡出液.和标准比色卡比对'测得它们的 pH分别为5.4.6. 3.6. 0. ④将形状.大小.质量相同的脂肪小块.分别放入盛有三种茶叶泡出液的相同杯中.在适宜的温度下保温5小时后.分别滤出脂肪块.吸干表面水分并称量.根据脂肪块在茶水中浸泡前后的质量变化.判定茶水能否溶解脂肪. 请回答下列问题: (1)以上实验操作步骤中错误的是 . (2)在第②步实验操作中“相同的条件主要是指:水的温度.茶叶的质量.冲泡的时间及 应相同. (3)组内有看的同学认为.第④步实验设计不严密.需要改进的是 .在第④步实验中. 根据实验的目的.适宜的温度应控制在 左右. (4)有人将茶水倒入有水垢的热水瓶中浸泡一下时间后振荡.发现水垢大部分消失了.产生这种现象的化学原理最可能是 . 答案:34. (1)③ (2)水的质量或体积 (3)要设置对照实验.37℃ (4)茶水呈酸性.与水垢中的碳酸盐等物质发生反应
网址:http://m.1010jiajiao.com/timu3_id_22829[举报]
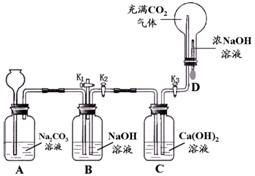 32、某化学兴趣小组设计了如图所示实验装置,进行了以下实验.
32、某化学兴趣小组设计了如图所示实验装置,进行了以下实验.(1)先打开K1,关闭K2和K3,从长颈漏斗向A 中加入足量的稀盐酸.此时装置B中发生反应的化学方程式为
CO2+2NaOH=Na2CO3+H2O
,打开K1的目的是防止B中气压过大,将瓶塞顶起
.(2)然后关闭K1和 K3,打开K2,将胶头滴管中的浓氢氧化钠溶液挤入锥形瓶中.稍后打开K3,此时装置C和D中的现象分别是
C中的液体流入D中,B中的液体流入C中,C中澄清的石灰水变浑浊
、C中的液体流入D中形成喷泉,D中溶液变浑浊
,装置C中发生反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.若在(2)实验过程中没有关闭K1,其它操作相同,则装置B的现象不同点是关闭K1,装置B中左侧导管末端能看到气泡;打开K1,则看不到该现象
.根据图1回答问题.
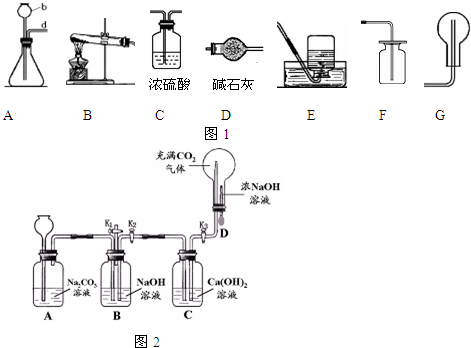
(1)写出仪器的名称:b
(2)实验室制取二氧化碳的化学方程式是
(3)氨气是一种无色、有刺激性气味的气体,极易溶于水,氨水显碱性.实验室用加热氯化铵和熟石灰两种固体的混合物来制取氨气,实验室制取氨气的发生、干燥、收集装置应分别选用(填序号)
(4)某化学兴趣小组设计了如图2所示实验装置,进行了以下实验.
①先打开K1,关闭K2和K3,从长颈漏斗向A 中加入足量的稀盐酸.此时装置B中发生反应的化学方程式为
②然后关闭K1和 K3,打开K2,将胶头滴管中的浓氢氧化钠溶液挤入锥形瓶中.稍后打开K3,此时装置C和D中的现象分别是
查看习题详情和答案>>

(1)写出仪器的名称:b
长颈漏斗
长颈漏斗
.(2)实验室制取二氧化碳的化学方程式是
CaCO3+2HCl═CaCl2+CO2↑+H2O
CaCO3+2HCl═CaCl2+CO2↑+H2O
,发生装置和气体的收集装置是AF
AF
(填装置序号,下同)(3)氨气是一种无色、有刺激性气味的气体,极易溶于水,氨水显碱性.实验室用加热氯化铵和熟石灰两种固体的混合物来制取氨气,实验室制取氨气的发生、干燥、收集装置应分别选用(填序号)
B
B
、D
D
、G
G
.(4)某化学兴趣小组设计了如图2所示实验装置,进行了以下实验.
①先打开K1,关闭K2和K3,从长颈漏斗向A 中加入足量的稀盐酸.此时装置B中发生反应的化学方程式为
CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
,打开K1的目的是防止B中气压过大,将瓶塞顶起
防止B中气压过大,将瓶塞顶起
.②然后关闭K1和 K3,打开K2,将胶头滴管中的浓氢氧化钠溶液挤入锥形瓶中.稍后打开K3,此时装置C和D中的现象分别是
C中的液体流入D中,B中的液体流入C中,C中澄清的石灰水变浑浊
C中的液体流入D中,B中的液体流入C中,C中澄清的石灰水变浑浊
、C中的液体流入D中形成喷泉,D中溶液变浑浊
C中的液体流入D中形成喷泉,D中溶液变浑浊
,装置C中发生反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
. 工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图所示
工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图所示(1)A、B处发生的现象分别是:A
红色粉末逐渐变黑
红色粉末逐渐变黑
、B澄清的石灰水变浑浊
澄清的石灰水变浑浊
;(2)为了防止溶液倒吸,本实验停止加热前是否要先断开A和B的连接处?
不需要
不需要
(填“需要”或“不需要”)(3)检验A中生成的固体粉末的方法是:
用磁铁吸附
用磁铁吸附
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品的质量/g | 166.5 | 166.3 | 166.1 | 166.1 |
记录如表.求:①反应中产生氢气
0.4
0.4
克;②生铁中含铁的质量分数.(结果精确到0.1%)(写出详细计算过程)
(5)某钢铁厂用480t含氧化铁为80%的赤铁矿石为原料,理论上能练的含杂质4%的生铁多少吨?(写出计算过程)