摘要:27.在一定温度下的密闭容器中存在如下反应:2SO2(g)+ O2 (g) 2SO3(g).已知c始(SO2)=0.4mol/L.c始(O2)=1mol/L.经测定该反应在该温度下的平衡常数K=19.判断:当SO2转化率为50%时.该反应是否达到平衡状态.若未达到.向哪个方向进行? 班级: 姓名: 考号:10位 学号:2位 鹤岗一中2009-2010学年度下学期期末考试 高一化学试题
网址:http://m.1010jiajiao.com/timu3_id_219145[举报]
在一定温度下的密闭容器中存在如下反应:2SO2(g)+O2 (g)?2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19.判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)
查看习题详情和答案>>
(5分)在一定温度下的密闭容器中存在如下反应:2SO2(g)+ O2 (g) 2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19。判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)
查看习题详情和答案>>
在一定温度下的密闭容器中存在如下反应2SO2(g)+O2(g)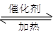 2SO3(g),已知c(SO2)始=0.4 mol·L-1,c(O2)始=1 mol·L-1,经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为 ( )
2SO3(g),已知c(SO2)始=0.4 mol·L-1,c(O2)始=1 mol·L-1,经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为 ( )
| A.0.24 mol·L-1 | B.0.28 mol·L-1 |
| C.0.32 mol·L-1 | D.0.26 mol·L-1 |
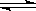 2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19。判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)
2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19。判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)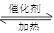 2SO3(g),已知c(SO2)始=0.4
mol·L-1,c(O2)始=1
mol·L-1,经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为 ( )
2SO3(g),已知c(SO2)始=0.4
mol·L-1,c(O2)始=1
mol·L-1,经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为 ( )