题目内容
在一定温度下的密闭容器中存在如下反应2SO2(g)+O2(g)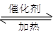 2SO3(g),已知c(SO2)始=0.4 mol·L-1,c(O2)始=1 mol·L-1,经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为 ( )
2SO3(g),已知c(SO2)始=0.4 mol·L-1,c(O2)始=1 mol·L-1,经测定该反应在该温度下的平衡常数K=19,则此反应中SO2的转化量为 ( )
| A.0.24 mol·L-1 | B.0.28 mol·L-1 |
| C.0.32 mol·L-1 | D.0.26 mol·L-1 |
C
解析试题分析: 2SO2(g)+O2(g)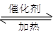 2SO3(g)
2SO3(g)
起始浓度(mol/L) 0.4 1 0
转化浓度(mol/L) 2x x 2x
平衡浓度(mol/L)0.4-2x 1-x 2x
所以有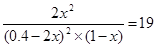
解得x=0.16mol/L
则此反应中SO2的转化量为2x=0.32mol/L
即答案选C。
考点:考查平衡常数的应用和可逆反应的有关计算
点评:该题是中等难度的试题,主要是考查学生对平衡常数的理解掌握程度,有助于培养学生的逻辑推理能力。该题的关键是让学生明确在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目
在一定温度下的定容密闭容器中,下列事实表明反应:A(s)+2B(g)?C(g)+D(g)已达平衡状态的是?( )
| A、混合气体的压强不变 | B、B的正反应速率与C的逆反应速率之比为2:1 | C、A的物质的量浓度不变 | D、单位时间内生成2 molB,同时消耗1 molC |
 2NH3(g)已经达到平衡状态的是
2NH3(g)已经达到平衡状态的是 2NH3(g)达到平衡状态的有
2NH3(g)达到平衡状态的有 2HI(g)达到平衡状态的有
2HI(g)达到平衡状态的有 N2O4(g)达到平衡状态的有
N2O4(g)达到平衡状态的有 CO(g)+H2(g)达到平衡状态的有
CO(g)+H2(g)达到平衡状态的有