摘要:某化学活动小组的同学在探究金属与酸反应时.发现铜与浓硫酸在加热条件下能够发生反应.并产生大量气体. [提出问题]产生气体的成分是什么呢? [分析讨论]经分析讨论.大家认为产生的气体可能是H2.SO2.SO3.O2等气体.经进一步查验后确认没有SO3.O2.于是大家决定进一步探究气体成分. [提出猜想]猜想①:产生的气体仅为SO2,猜想②:产生的气体仅为H2,你认为猜想③ . [查阅资料] SO2是一种有毒气体.不能燃烧.能使红色的品红溶液变为无色.是一种主要大气污染物.H2则不能使红色品红溶液褪色.铜与浓硫酸反应时.硫酸总会剰余. [设计实验]该小组的同学据此设计并完成了如图所示的实验: [分析与结论] (1)图中X为 溶液. (2)由以上实验可知:猜想 正确. [反思与评价] (3)与活泼金属和稀硫酸的反应不同.铜与浓硫酸反应时.硫元素的化合价 . (4)实验结束后.有同学认为在处理图中反应①试管中残液时.应先用水将残液稀释.正确的操作方法是 . (5)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中.其原因是 .
网址:http://m.1010jiajiao.com/timu3_id_21807[举报]
某化学活动小组的同学在探究金属与酸反应时,发现铜与浓硫酸在加热条件下能够发生反应,并产生大量气体.
[提出问题]产生气体的成分是什么呢?
[分析讨论]经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分.
[提出猜想]猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;你认为猜想③______.
[查阅资料]SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物.H2则不能使红色品红溶液褪色.铜与浓硫酸反应时,硫酸总会剰余.
[设计实验]该小组的同学据此设计并完成了如图所示的实验
[分析与结论]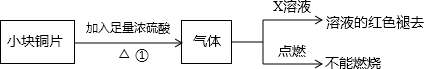
(1)图中X为______溶液.
(2)由以上实验可知:猜想______(填①、②、③)正确.
[反思与评价]
(3)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价______.
(4)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是______.
(5)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是______.
查看习题详情和答案>>
某化学活动小组的同学在探究金属与酸反应时,发现铜与浓硫酸在加热条件下能够发生反应,并产生大量气体.
[提出问题]产生气体的成分是什么呢?
[分析讨论]经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分.
[提出猜想]猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;你认为猜想③______.
[查阅资料]SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物.H2则不能使红色品红溶液褪色.铜与浓硫酸反应时,硫酸总会剰余.
[设计实验]该小组的同学据此设计并完成了如图所示的实验
[分析与结论]
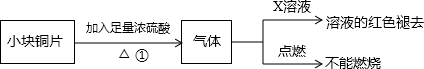
(1)图中X为______溶液.
(2)由以上实验可知:猜想______(填①、②、③)正确.
[反思与评价]
(3)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价______.
(4)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是______.
(5)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是______.
查看习题详情和答案>>
[提出问题]产生气体的成分是什么呢?
[分析讨论]经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分.
[提出猜想]猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;你认为猜想③______.
[查阅资料]SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物.H2则不能使红色品红溶液褪色.铜与浓硫酸反应时,硫酸总会剰余.
[设计实验]该小组的同学据此设计并完成了如图所示的实验
[分析与结论]

(1)图中X为______溶液.
(2)由以上实验可知:猜想______(填①、②、③)正确.
[反思与评价]
(3)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价______.
(4)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是______.
(5)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是______.
某化学活动小组的同学在探究金属与酸反应时,发现铜与浓硫酸在加热条件下能够发生反应,并产生大量气体。 [提出问题]产生气体的成分是什么呢?
[分析讨论]经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分。
[提出猜想](1)猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;
你认为猜想③ 。
[查阅资料] SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物。
H2则不能使红色品红溶液褪色。铜与浓硫酸反应时,硫酸总会剰余。
[设计实验]该小组的同学据此设计并完成了如图所示的实验:
[分析讨论]经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分。
[提出猜想](1)猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;
你认为猜想③ 。
[查阅资料] SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物。
H2则不能使红色品红溶液褪色。铜与浓硫酸反应时,硫酸总会剰余。
[设计实验]该小组的同学据此设计并完成了如图所示的实验:

[分析与结论]
(2)图中X为 溶液。
(3)由以上实验可知:猜想 (填①、②、③)正确。
[反思与评价]
(4)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价 。
(5)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是 。
(6)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是 。
查看习题详情和答案>>
(2)图中X为 溶液。
(3)由以上实验可知:猜想 (填①、②、③)正确。
[反思与评价]
(4)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价 。
(5)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是 。
(6)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是 。
某化学活动小组的同学在探究金属与酸反应时,发现铜与浓硫酸在加热条件下能够发生反应,并产生大量气体。
【提出问题】产生气体的成分是什么呢?
【分析讨论】经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分。
【提出猜想】猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;你认为猜想③ 。
【查阅资料】SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物。H2则不能使红色品红溶液褪色。铜与浓硫酸反应时,硫酸总会剰余。
【设计实验】该小组的同学据此设计并完成了如图所示的实验:
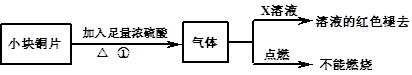
【分析与结论】
(1)图中X为 溶液。
(2)由以上实验可知:猜想 (填①、②、③)正确。
【反思与评价】
(3)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价 。
(4)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是 。
(5)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是 。
查看习题详情和答案>>
某化学活动小组的同学在探究金属与酸反应时,发现铜与浓硫酸在加热条件下能够发生反应,并产生大量气体。
【提出问题】产生气体的成分是什么呢?
【分析讨论】经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分。
【提出猜想】猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;你认为猜想③ 。
【查阅资料】 SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物。H2则不能使红色品红溶液褪色。铜与浓硫酸反应时,硫酸总会剰余。
【设计实验】该小组的同学据此设计并完成了如图所示的实验:

【分析与结论】
(1)图中X为 溶液。
(2)由以上实验可知:猜想 (填①、②、③)正确。
【反思与评价】
(3)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价 。
(4)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是 。
(5)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是 。 查看习题详情和答案>>
【提出问题】产生气体的成分是什么呢?
【分析讨论】经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分。
【提出猜想】猜想①:产生的气体仅为SO2;猜想②:产生的气体仅为H2;你认为猜想③ 。
【查阅资料】 SO2是一种有毒气体,不能燃烧,能使红色的品红溶液变为无色,是一种主要大气污染物。H2则不能使红色品红溶液褪色。铜与浓硫酸反应时,硫酸总会剰余。
【设计实验】该小组的同学据此设计并完成了如图所示的实验:

【分析与结论】
(1)图中X为 溶液。
(2)由以上实验可知:猜想 (填①、②、③)正确。
【反思与评价】
(3)与活泼金属和稀硫酸的反应不同,铜与浓硫酸反应时,硫元素的化合价 。
(4)实验结束后,有同学认为在处理图中反应①试管中残液时,应先用水将残液稀释,正确的操作方法是 。
(5)另有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,其原因是 。 查看习题详情和答案>>