摘要:将锌片和铜片用导线相连(导线中间接入一个电流表)平行插入盛有稀硫酸的烧杯中进行实验.完成下列表格 实验现象 反应的方程式 锌片逐渐 , 铜片上有 . 负极: 片.电极方程式是: 正极: 片.电极方程式是: 电流表指针 外电路中电子的流动方向是:
网址:http://m.1010jiajiao.com/timu3_id_215644[举报]
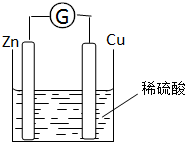 将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:(1)锌片上发生的电极反应:
Zn-2e-=Zn2+
Zn-2e-=Zn2+
;铜片上发生的电极反应:2H++2e-=H2↑
2H++2e-=H2↑
;(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况氢气的体积为多少L?(请写出计算过程)
4.48L
4.48L
.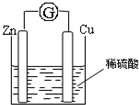 将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图,总反应为:Zn+2H+=Zn2++H2↑回答下列问题:
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图,总反应为:Zn+2H+=Zn2++H2↑回答下列问题:(1)锌片上发生的电极反应:
铜片上发生的电极反应:
(2)工作一段时间后,锌片的质量减少13g,试计算产生标准状况氢气的体积为多少?(请写出计算过程)
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:
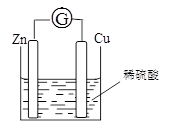
(1) 锌片上发生的电极反应: ;
铜片上发生的电极反应: ;
(2)若该电池中两电极的总质量为60g,工作一段时间后,
取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况
氢气的体积为多少L?
查看习题详情和答案>>