摘要:23. f a b c d e A B C D (1)在上面元素周期表中全部是金属元素的区域为 . (2)在上面元素周期表中元素a.b.c.d.e.f中气态氢化物最稳定的化合物是 .化学性质最不活泼的元素为 .a.b.c元素的简单离子中半径由大到小的顺序为 . ①c离子的结构示意图为 . d原子的结构示意图为 . ②写出c.a形成的原子个数1:1的化合物及 f的氢化物的电子式 (3)现有甲.乙两种短周期元素.室温下.甲元素单质在冷的浓硫酸或空气中.表面都生成致密的氧化膜.乙元素原子核外M电子层与K电子层上的电子数相等. ①用元素符号将甲.乙两元素填写在上面元素周期表中对应的位置. ②甲.乙两元素相比较.金属性较强的是 .可以验证该结论的实验是 . a 将在空气中放置已久的这两种元素的块状单质分别放入热水中 b 将这两种元素的单质粉末分别和同浓度的盐酸反应 c 将这两种元素的单质粉末分别和热水作用.并滴入酚酞溶液 d 比较这两种元素的气态氢化物的稳定性
网址:http://m.1010jiajiao.com/timu3_id_214687[举报]

(1)在上面元素周期表中全部是金属元素的区域为
b
b
(a)A (b)B (c)C (d)D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲、乙两元素相比较,金属性较强的是
Mg
Mg
(填名称),可以验证该结论的实验是
bc
bc
.(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
③写出甲的氧化物及氧化物对应水化物分别与强碱反应的离子方程式
Al2O3 +2OH-═2AlO2-+H2O
Al2O3 +2OH-═2AlO2-+H2O
、Al(OH)3 +OH-═AlO2-+2H2O
Al(OH)3 +OH-═AlO2-+2H2O
.(3)表中所列小写字母分别代表一种化学元素:
①m、f、j的单质熔点由高到低的顺序
C>Si>P
C>Si>P
(填元素符号).②以上元素形成的金属单质中,熔点最低的是
Na
Na
(填元素符号).③f、m、n、g所形成的氢化物的稳定性还性由强到弱的顺序为
HCl、H2S、PH3、SiH4
HCl、H2S、PH3、SiH4
(填化学式);④甲、乙、c、d、e形成的简单离子的半径由小到大的顺序为
Al3+、Mg2+、Na+、O2-、N3-
Al3+、Mg2+、Na+、O2-、N3-
.⑤f元素单质是在生产中用量很大,试写出工业上制备f元素单质的化学方程式
SiO2+2C
2CO+Si
| ||
SiO2+2C
2CO+Si
.
| ||
⑥c元素的单质用途
氮气是合成氨、制硝酸的重要原料;由于其性质稳定常被用作保护气;在高科技领域中常用液氮制造低温环境
氮气是合成氨、制硝酸的重要原料;由于其性质稳定常被用作保护气;在高科技领域中常用液氮制造低温环境
(填一条).
(1)在上面元素周期表中全部是金属元素的区域为
(b)
(b)
.(a)A (b)B (c)C (d)D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
(3)表中所列小写字母分别代表一种化学元素:①f、m、n、g所形成的氢化物的稳定性还原性由强到弱的顺序为
HCl>H2S>PH3>SiH4
HCl>H2S>PH3>SiH4
(填化学式);②甲、乙、c、d、e形成的简单离子的半径由小到大的顺序为
Al3+、Mg2+、Na+、O2-、N3-
Al3+、Mg2+、Na+、O2-、N3-
.(离子用实际离子符号表示)③f的最高价氧化物制备对应的水化物的化学方程式
SiO2+2NaOH=Na2SiO3+H2O;Na2SiO3+2HCl═2NaCl+H2SiO3↓;
SiO2+2NaOH=Na2SiO3+H2O;Na2SiO3+2HCl═2NaCl+H2SiO3↓;
④c元素的单质用途
氮气是一种重要的工业原料,化学性质稳定,可做保护气
氮气是一种重要的工业原料,化学性质稳定,可做保护气
(填一条).(14分)元素周期表是学习化学的重要工具,它隐含着许多信息和规律,下面是八种短周期元素的相关信息(已知铍的原子半径为0.089nm)
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(1)B元素在元素周期表中的位置___________________,上述八种元素的最高价氧化物对应的水化物中酸性最强的是__________,A离子的结构示意图_______________。
(2)用电子式表示A、D形成化合物的过程:____________________________________。H、E形成原子个数比为1:1的化合物的电子式为___________,含有的化学键类型为____________。C2D2的电子式为______________________。
(3)下列说法能说明D的非金属性比C强的选项____________
①H2CO4比HDO稳定②HDO4比H2CO4酸性强③C2-比D-易被氧化④HD比H2C稳定⑤铜与HD不反应,但能与浓H2CO4反应⑥铁与D2加热生成FeD3,铁与C加热生成FeC⑦C原子与D原子电子层数相同,D原子半径小于C原子。
A、全部 B、②③④⑥⑦ C、①②④⑤⑥ D、除①以外
(4)A、B、C、D、E形成的简单离子半径由大到小的顺序为_______________________。(用具体离子符号表示)
(5)C单质与H的最高价氧化物对应水化物在加热条件下能发生反应,若有3mol的C参与反应,转移4NA的电子,请写出离子反应方程_______________________________________,氧化剂与还原剂的质量之比_____________________。 查看习题详情和答案>>
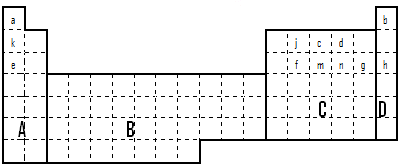
(1)在上面元素周期表中全部是金属元素的区域为______.
(a)A (b)B (c)C (d)D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
(3)表中所列小写字母分别代表一种化学元素:①f、m、n、g所形成的氢化物的稳定性还原性由强到弱的顺序为______(填化学式);
②甲、乙、c、d、e形成的简单离子的半径由小到大的顺序为______.(离子用实际离子符号表示)
③f的最高价氧化物制备对应的水化物的化学方程式______
④c元素的单质用途______(填一条).
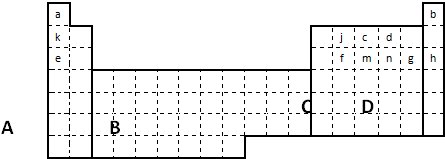
(1)在上面元素周期表中全部是金属元素的区域为______
(a)A (b)B (c)C (d)D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲、乙两元素相比较,金属性较强的是______(填名称),可以验证该结论的实
验是______.
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
③写出甲的氧化物及氧化物对应水化物分别与强碱反应的离子方程式
______、______.
(3)表中所列小写字母分别代表一种化学元素:
①m、f、j的单质熔点由高到低的顺序______(填元素符号).
②以上元素形成的金属单质中,熔点最低的是______(填元素符号).
③f、m、n、g所形成的氢化物的稳定性还性由强到弱的顺序为______(填化学式);
④甲、乙、c、d、e形成的简单离子的半径由小到大的顺序为______.
⑤f元素单质是在生产中用量很大,试写出工业上制备f元素单质的化学方程式______.
⑥c元素的单质用途______(填一条).