摘要:下列说法中.正确的是( ) ①在第三周期中.随着原子序数的递增.元素的性质呈周期性变化 ②同位素原子的化学性质几乎完全相同.而物理性质不同 ③同一元素不可能既表现金属性.又表现非金属性 ④元素的性质呈周期性变化的根本原因是核外电子排布的周期性变化 ⑤同一主族元素的原子.最外层电子数相同.它们化学性质也完全相同 ⑥电子层结构相同的粒子.化学性质完全相同 ⑦非金属元素的原子最外层电子数都大于4.在反应中都易得电子 ⑧短周期元素X.Y.Z在周期表中的位置如图.则非金属性:Y>Z>X A. ②④⑧ B. ①②③ C. ①④⑧ D. ③⑤⑥
网址:http://m.1010jiajiao.com/timu3_id_214305[举报]
下列说法中,正确的是
[ ]
①在第三周期中,随着原子序数的递增,元素的性质呈周期性变化
②同位素原子的化学性质几乎完全相同,而物理性质不同
③同一元素不可能既表现金属性,又表现非金属性
④元素的性质呈周期性变化的根本原因是核外电子排布的周期性变化
⑤同一主族元素的原子,最外层电子数相同,它们化学性质也完全相同
⑥电子层结构相同的粒子,化学性质完全相同
⑦非金属元素的原子最外层电子数都大于4,在反应中都易得电子
⑧短周期元素X、Y、Z在周期表中的位置如图,则非金属性:Y>Z>X
②同位素原子的化学性质几乎完全相同,而物理性质不同
③同一元素不可能既表现金属性,又表现非金属性
④元素的性质呈周期性变化的根本原因是核外电子排布的周期性变化
⑤同一主族元素的原子,最外层电子数相同,它们化学性质也完全相同
⑥电子层结构相同的粒子,化学性质完全相同
⑦非金属元素的原子最外层电子数都大于4,在反应中都易得电子
⑧短周期元素X、Y、Z在周期表中的位置如图,则非金属性:Y>Z>X

A.②④⑧
B.①②③
C.①④⑧
D.③⑤⑥
查看习题详情和答案>>
B.①②③
C.①④⑧
D.③⑤⑥
有四种短周期元素的部分性质如下,请根据有关信息填空:
注:气体密度已换算为标准状况
(1)元素W在周期表中的位置
(2)短周期主族元素中,元素X以及与其相邻元素的气态氢化物的稳定性由强到弱顺序是:
(3)同族元素单质及其化合物在许多性质上都存在着递变规律.下列有关说法正确的是
a.元素W所在族,随着原子序数递增,单质的熔点逐渐降低
b.元素X所在族,随着原子序数递增,对应简单离子的还原性逐渐增强
c.元素Y所在族,随着原子序数递增,对应氢化物的沸点逐渐升高
d.元素Z所在族,随着原子序数递增,最高氧化物对应水化物的酸性逐渐增强
(4)Z单质与足量Y单质反应,生成物的电子式为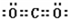
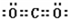 ,已知生成1mol该产物将伴随393.51kJ的热量变化,写出该反应的热化学方程式
,已知生成1mol该产物将伴随393.51kJ的热量变化,写出该反应的热化学方程式
查看习题详情和答案>>
| 元素 | W | X | Y | Z |
| 原子半径 | 186pm | 99pm | 66pm | 77pm |
| 核外电子 | 有4种能级不同的电子 | 最外层有7种运动状态不同的电子 | 核外电子占有5个轨道 | 有2个未成对电子 |
| 单质 部分 性质 |
密度:0.97g?cm-3 熔点:97.8℃ 能导电 |
沸点:-34.0℃ 不能导电 |
密度:1.43g?L-1 沸点:-183.0℃ 不能导电 |
熔点:3550℃ 能导电 |
(1)元素W在周期表中的位置
第三周期第ⅠA族
第三周期第ⅠA族
,根据性质描述,元素Z的单质是石墨
石墨
(写名称),上述元素的简单离子中半径最小的是Na+
Na+
(写离子符号).(2)短周期主族元素中,元素X以及与其相邻元素的气态氢化物的稳定性由强到弱顺序是:
HF>HCl>H2S
HF>HCl>H2S
(用化学式表示).(3)同族元素单质及其化合物在许多性质上都存在着递变规律.下列有关说法正确的是
b
b
(选填序号).a.元素W所在族,随着原子序数递增,单质的熔点逐渐降低
b.元素X所在族,随着原子序数递增,对应简单离子的还原性逐渐增强
c.元素Y所在族,随着原子序数递增,对应氢化物的沸点逐渐升高
d.元素Z所在族,随着原子序数递增,最高氧化物对应水化物的酸性逐渐增强
(4)Z单质与足量Y单质反应,生成物的电子式为
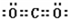
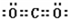
C(s)+O2(g)=CO2△H=-393.51kJ/mol
C(s)+O2(g)=CO2△H=-393.51kJ/mol
.下列说法中正确的是( )
A.元素性质随着相对原子质量的递增而呈周期性的变化叫元素周期律
B.同周期第ⅡA族与第IIIA族的元素原子序数之差可能为1、11或25
C.在周期表中ⅠA族处寻找催化剂和耐高温的合金材料
D.第三周期元素的离子半径,从左到右逐渐减小
查看习题详情和答案>>下列说法中正确的是( )
A.元素性质随着相对原子质量的递增而呈周期性的变化叫元素周期律
B.同周期第ⅡA族与第IIIA族的元素原子序数之差可能为1、11或25
C.在周期表中ⅠA族处寻找催化剂和耐高温的合金材料
D.第三周期元素的离子半径,从左到右逐渐减小
查看习题详情和答案>>|
下列说法中正确的是 | |
| [ ] | |
A. |
元素性质随着相对原子质量的递增而呈周期性的变化叫元素周期律 |
B. |
同周期第ⅡA族与第IIIA族的元素原子序数之差可能为1、11或25 |
C. |
在周期表中ⅠA族处寻找催化剂和耐高温的合金材料 |
D. |
第三周期元素的离子半径,从左到右逐渐减小 |