摘要:18.下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数.Y为元素的有关性质).请把与下面元素有关性质相符的曲线标号填入相应的空格中:19.元素X.Y.Z.W均为短周期元素.且原子序数依次增大.已知Y原子最外层电子数占核外电子总数的3/4.W-.Z+.X+半径逐渐减小.化合物XW常温下为气体.Z是本周期中除稀有气体元素外.原子半径最大的元素.据此回答下列问题: (1)W在元素周期表中的位置是 .实验室制取W单质的离子方程式为 . (2)A.B均为由上述四种元素中的三种组成的强电解质.组成元素的原子数目比均为1:1:1.若为强碱.则A的电子式是 . B的化学式是 . (3)C是由上述四种元素中的两种组成的一种含有非极性键的离子化合物.则C的名称为为 . (4)用B在碱性条件下可以处理含CN-的工业废水.请将下列6种微粒:CN-..N2.OH-.B中阴离子.W的阴离子.分别填入下面对应的横线上.组成一个配平的离子方程式: + + = + + + (5)X与Y形成的18电子分子与同样是18电子分子的H2S在水溶液中反应生成一种单质的化学方程式 .可观察到的实验现象是
网址:http://m.1010jiajiao.com/timu3_id_214023[举报]
下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
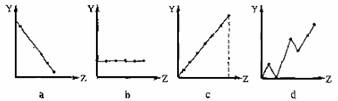
①ⅡA族元素的在外层电子数 。
②第3周期元素的最高化合价 。
③F-、 Na+ 、Mg2+、Al3+的离子半径 。
查看习题详情和答案>>(1)下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数,Y为元素的有关性质).
请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数
②第3周期元素的最高化合价
③F-、Na+、Mg2+、Al3+的离子半径
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度最小,则化合物A中的化学键类型为
③Z与M形成的稳定固体化合物的电子式为
 .
.
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式
查看习题详情和答案>>

请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数
b
b
.②第3周期元素的最高化合价
c
c
.③F-、Na+、Mg2+、Al3+的离子半径
a
a
.(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是
HClO4
HClO4
.②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度最小,则化合物A中的化学键类型为
离子键、(极性)共价键
离子键、(极性)共价键
,若B为常见家用消毒剂的主要成分,则B的化学式是NaClO
NaClO
.③Z与M形成的稳定固体化合物的电子式为


④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式
H2O2+H2S=S↓+2H2O
H2O2+H2S=S↓+2H2O
,可观察到的实验现象是无色溶液中产生淡黄色浑浊
无色溶液中产生淡黄色浑浊
.(1)下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数,Y为元素的有关性质).
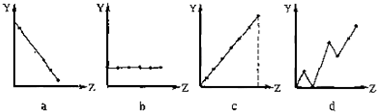
请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数______.
②第3周期元素的最高化合价______.
③F-、Na+、Mg2+、Al3+的离子半径______.
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是______.
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度最小,则化合物A中的化学键类型为______,若B为常见家用消毒剂的主要成分,则B的化学式是______.
③Z与M形成的稳定固体化合物的电子式为______.
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式______,可观察到的实验现象是______.
查看习题详情和答案>>

请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数______.
②第3周期元素的最高化合价______.
③F-、Na+、Mg2+、Al3+的离子半径______.
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是______.
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度最小,则化合物A中的化学键类型为______,若B为常见家用消毒剂的主要成分,则B的化学式是______.
③Z与M形成的稳定固体化合物的电子式为______.
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式______,可观察到的实验现象是______.
(1)下列曲线分别表示元素的某种性质与该电荷数的关系(Z为该电荷数,Y为元素的有关性质).
请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数 .
②第3周期元素的最高化合价 .
③F-、Na+、Mg2+、Al3+的离子半径 .
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是 .
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度最小,则化合物A中的化学键类型为 ,若B为常见家用消毒剂的主要成分,则B的化学式是 .
③Z与M形成的稳定固体化合物的电子式为 .
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式 ,可观察到的实验现象是 . 查看习题详情和答案>>

请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数 .
②第3周期元素的最高化合价 .
③F-、Na+、Mg2+、Al3+的离子半径 .
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M原子的最外层电子数与次外电子数之比为3:4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①N的最高价氧化物的水化物的化学式是 .
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度最小,则化合物A中的化学键类型为 ,若B为常见家用消毒剂的主要成分,则B的化学式是 .
③Z与M形成的稳定固体化合物的电子式为 .
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质的化学方程式 ,可观察到的实验现象是 . 查看习题详情和答案>>
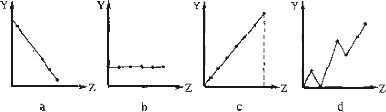
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质).请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数________.
②第3周期元素的最高化合价________.
③F-、Na+、Mg2+、Al3+的离子半径________.
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①Y和M形成的常见化合物的化学式是________.
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为________,B的化学式是________.
③Z与Y形成的稳定化合物的电子式为________.
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成M单质的化学方程式:________该反应中转移的电子数目为________.