摘要:元素周期表是我们学习和研究化学的重要工具.它的内容十分丰富.下面是元素周期表部分内容.请回答下列问题 1 H 氢 2 He 氦 2 3 Li 锂 4 Be 铍 5 B 硼 6 C 碳 7 N 氮 8 O 氧 9 F 氟 10Ne 氖 3 11Na 钠 12 镁 13 Al 铝 14 Si 硅 15 P 磷 16 S 硫 17 Cl 氯 18 Ar 氩 (1)在元素周期表中.原子序数为12的元素符号是 . 其原子结构示意图为 在化学反应中该原子易 (填“得到 或“失去 )电子. (2)写出原子序数为1.6.8.11四种元素所组成化合物的化学式 . (3)通过分析.同一横行元素之间的排列有一定的规律.例如: ①从左到右.由金属元素逐渐向非金属元素过渡, ②从左到右.各元素原子的电子层数相同, ③ .
网址:http://m.1010jiajiao.com/timu3_id_21275[举报]
元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题
(1)从表中可查出硅元素的相对原子质量为
(2)6~11号元素中属于金属元素的有
(3)表中不同元素最本质的区别是
(4)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③
(5)请简述用高锰酸钾制氧气前,检验装置气密性的方法.
(6)用微粒的观点解释混合物与纯净物有什么不同.
查看习题详情和答案>>
| 1 H 1.008 |
2 He 4.003 | |||||||
| 3 Li 6.941 |
4 Be 9.012 |
5 B 10.81 |
6 C 12.01 |
7 N 14.01 |
8 O 16.00 |
9 F 19.00 |
10 Ne 20.18 | |
| 11 Na 22.99 |
12 Mg 24.31 |
… | 13 Al 26.98 |
14 Si 28.09 |
15 P 30.97 |
16 S 32.06 |
17 Cl 35.45 |
18 Ar 39.95 |
28.09
28.09
.(2)6~11号元素中属于金属元素的有
Na
Na
(填元素符号).(3)表中不同元素最本质的区别是
质子数不同
质子数不同
.(4)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③
最外层的电子数依次增加
最外层的电子数依次增加
(任写一条).(5)请简述用高锰酸钾制氧气前,检验装置气密性的方法.
先将导管伸入液面下,用手紧握试管,观察到烧杯内导管口有气泡冒出,松开手后,导管内有一段上升液柱,说明该装置气密性良好.
先将导管伸入液面下,用手紧握试管,观察到烧杯内导管口有气泡冒出,松开手后,导管内有一段上升液柱,说明该装置气密性良好.
(6)用微粒的观点解释混合物与纯净物有什么不同.
由分子构成的物质,由同种分子构成的属于纯净物,由不同种分子构成的属于混合物
由分子构成的物质,由同种分子构成的属于纯净物,由不同种分子构成的属于混合物
.元素周期表是我们学习和研究化学的重要工具.如图是元素周期表中1---18号元素原子的核外电子排布,我们对它进行研究:
(1)第17号元素的名称是
(2)从上表中我们还可以探究出以下规律:
①原子序数与原子核电荷数在数值上相等;
②
③
④
查看习题详情和答案>>
| 第一周期 | 1 H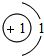 |
2 He | ||||||
| 第二周期 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne |
| 第三周期 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl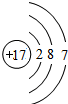 |
18 Ar |
氯
氯
,它属于非金属
非金属
元素(填“金属”或“非金属”),它在化学反应中容易得
得
(填“得”或“失”)电子.(2)从上表中我们还可以探究出以下规律:
①原子序数与原子核电荷数在数值上相等;
②
同周期元素原子的电子层数相同
同周期元素原子的电子层数相同
;③
同一族元素原子最外层电子数相同
同一族元素原子最外层电子数相同
;④
随着核电荷数的递增,元素原子最外层电子的排布呈现周期性的变化
随着核电荷数的递增,元素原子最外层电子的排布呈现周期性的变化
.元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.
(1)从表中可查出硅元素的相对原子质量为
(2)光纤的主要成分是14号元素和8号元素形成的化合物.请写出其化学式
(3)通过分析,同一横行元素之间的排列有一定的规律
(4)如图是几种微粒结构示意图,其中具有相似的化学性质的是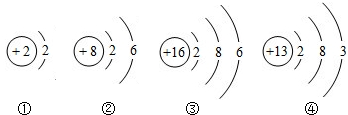
(5)市场上销售的“高钙牛奶”、“含氟牙膏”、“加碘盐”中的“钙、氟、碘”等所指的是
查看习题详情和答案>>
| 1 H 1.008 |
2 He 4.003 | |||||||
| 3 Li 6.941 |
4 Be 9.012 |
5 B 10.81 |
6 C 12.01 |
7 N 14.01 |
8 O 16.00 |
9 F 19.00 |
10 Ne 20.18 | |
| 11 Na 22.99 |
12 Mg 24.31 |
… | 13 Al 26.98 |
14 Si 28.09 |
15 P 30.97 |
16 S 32.06 |
17 Cl 35.45 |
18 Ar 39.95 |
28.09
28.09
.11号元素的核电荷数11
11
.(2)光纤的主要成分是14号元素和8号元素形成的化合物.请写出其化学式
SiO2
SiO2
.(3)通过分析,同一横行元素之间的排列有一定的规律
从左至右原子序数依次递增等
从左至右原子序数依次递增等
(4)如图是几种微粒结构示意图,其中具有相似的化学性质的是
②③
②③
(填序号)
(5)市场上销售的“高钙牛奶”、“含氟牙膏”、“加碘盐”中的“钙、氟、碘”等所指的是
元素
元素
(选填“原子”、“元素”).元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题
(1)从表中可查出硅元素的相对原子质量为
(2)6~11号元素中属于金属元素的有
(3)表中不同种元素最本质的区别是其原子的
(4)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③
查看习题详情和答案>>
| 1 H 1.008 |
2 He 4.003 | |||||||
| 3 Li 6.941 |
4 Be 9.012 |
5 B 10.81 |
6 C 12.01 |
7 N 14.01 |
8 O 16.00 |
9 F 19.00 |
10 Ne 20.18 | |
| 11 Na 22.99 |
12 Mg 24.31 |
… | 13 Al 26.98 |
14 Si 28.09 |
15 P 30.97 |
16 S 32.06 |
17 Cl 35.45 |
18 Ar 39.95 |
28.09
28.09
.(2)6~11号元素中属于金属元素的有
Na
Na
(填元素符号).(3)表中不同种元素最本质的区别是其原子的
原子序数
原子序数
不同.(4)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③
从左到右,元素的原子最外层电子数依次递增
从左到右,元素的原子最外层电子数依次递增
(任写一条你发现的).元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富,图是某学生绘制的元素周期表的一部分:
请根据相关信息与知识回答:
(1)1869年俄国化学
(2)氦、氖、氩等稀有气体的化学性质很不活泼,其原因是
(3)用化学符号表示:氟元素
(4)图A是氮原子的原子结构示意图,则方框横线上的数字是

(5)请仔细阅读和观察上表,其中有一种元素的名称书写有误,请你写出其正确的元素名称
(6)通过分析,同一横行元素之间的排列有一定规律,例如
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③从左到右,
查看习题详情和答案>>
| 1 H 氢 |
 |
2 He 氦 | |||||
| 3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 氮 |
8 O 氧 |
9 氟 |
10 Ne 氖 |
| 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |
(1)1869年俄国化学
门捷列夫
门捷列夫
发现了元素周期律并绘制了元素周期表.(2)氦、氖、氩等稀有气体的化学性质很不活泼,其原因是
它们原子的最外层电子数均已达到稳定结构(最外层达到8个,氦最外层达到2个的稳定结构)
它们原子的最外层电子数均已达到稳定结构(最外层达到8个,氦最外层达到2个的稳定结构)
.(3)用化学符号表示:氟元素
F
F
,氮气N2
N2
.(4)图A是氮原子的原子结构示意图,则方框横线上的数字是
5
5
,图B表示的(写离子符号)Mg2+
Mg2+
.
(5)请仔细阅读和观察上表,其中有一种元素的名称书写有误,请你写出其正确的元素名称
碳
碳
,过量排放该元素的一种氧化物,会引起温室
温室
效应,使全球变暖,请列举其中一条防止该效应进一步增强的措施植树造林
植树造林
.(6)通过分析,同一横行元素之间的排列有一定规律,例如
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,各元素原子的电子层数相同;
③从左到右,
元素原子的最外层电子数逐渐增加
元素原子的最外层电子数逐渐增加
.