摘要:16.常见的气体干燥剂按酸碱性分类 A.酸性干燥剂:如浓硫酸.五氧化二磷.硅胶.酸性干燥剂能够干燥显酸性或中性的气体. 如 B.碱性干燥剂:如生石灰.碱石灰.固体氢氧化钠.能够干燥显碱性或中性的气体.如 C.中性干燥剂:如无水氯化钙.可以干燥中性.酸性.碱性气体.如 显碱性的气体不能选用酸性干燥剂.显酸性的气体不能选用碱性干燥剂有还原性的气体不能有氧化性的干燥剂.能与气体反应的物质不能用作干燥剂.如不能用氯化钙干燥氨气.不能用浓硫酸干燥氨气.硫化氢.溴化氢.碘化氢等气体净化与干燥注意事项:一般情况下若采用溶液作除杂试剂时.则是先除杂后干燥.若要用加热方法除去杂质时.则是先干燥再加热
网址:http://m.1010jiajiao.com/timu3_id_209432[举报]
A、B、C、D为四种常见元素,A的一种单质在雷雨天、静电复印时均可产生,常用于游泳池消毒;B的最高价氧化物对应水化物是一种常见的液态干燥剂。C、B同周期,C和A组成的一种化合物可用于呼吸面具供氧。D的单质常温下是深红棕色液体。
(1)写出A、C的元素符号:A_________________;C_________________。
(2)将A、B组成的气态化合物通入D单质的水溶液中,可观察到的现象是______________,写出发生反应的离子方程式,并标出电子转移方向和数目_____________________________。
(3)已知:B的气态氢化物的水溶液与A、B组成的气态化合物的水化物的水溶液均呈酸性。今欲确定这两种酸的酸性强弱,请你设计实验方案。
(4)试证明:B与D何种元素的非金属性更强。请用化学方程式表示你所设计实验的反应原理:____________________________________________________________________。
查看习题详情和答案>>如图为一些常见无机物之间的转化关系,其中常温下E是一种无色无味的液体,F是一种淡黄色粉末,G是一种无色无味的气体.请回答下列问题
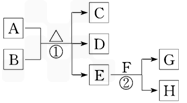
(1)F的电子式为__________________;在反应②中,每生成2.24 L(标准状况下)气体G,反应转移电子的数目为________ NA(NA代表阿伏加德罗常数的值).
(2)若A与B均为固体化合物,C是一种常见的中性干燥剂,写出反应①的化学方程式:__________________________________________.
(3)若C、D均为气体,且都能使澄清石灰水变浑浊,B、C、D、E中含有同种元素,则A与B分别为__________、______________(写名称).
查看习题详情和答案>>
(2)若A与B均为固体化合物,C是一种常见的中性干燥剂,写出反应①的化学方程式:__________________________________________.
(3)若C、D均为气体,且都能使澄清石灰水变浑浊,B、C、D、E中含有同种元素,则A与B分别为__________、______________(写名称).
活性亚铬酸铜催化剂在一定温度下,将NH3和NOx转变为N2和H2O,这是目前硝酸厂尾气治理所普遍采用的一种方法.某校化学研究小组拟验证NO能被氨气还原并计算其转化率.
将一定量硝酸铜溶液、重铬酸铵溶液与氨水作用得沉淀物(CuNH4(OH)CrO4),过滤、洗涤,80℃烘干12h,最后焙烧得活性亚铬酸铜催化剂.用得到的催化剂按下列流程进行实验(已知:浓硫酸在常温下不氧化NO气体).

根据题意完成下列各题:
(1)装置③可以选的干燥剂为: (选填序号,下同);装置④可以选的固体干燥剂为: .
A.浓硫酸 B.碱石灰 C.硅胶 D.无水氯化钙
(2)若实验室只提供浓氨水和生石灰两种试剂,你会选择下图 装置来制取氨气,发生反应的化学方程式为: ;
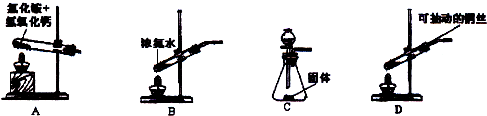
(3)若实验室提供稀硝酸、铜丝和小颗粒石灰石,若选用上图D装置制取较纯NO,其操作方法是: .
(4)装置⑥中,小段玻璃管的作用是 :
(5)装置⑦的作用可能是: ;
(6)若进入装置⑤的NO共2688mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下2016mL N2,则NO的转化率为: .
查看习题详情和答案>>
将一定量硝酸铜溶液、重铬酸铵溶液与氨水作用得沉淀物(CuNH4(OH)CrO4),过滤、洗涤,80℃烘干12h,最后焙烧得活性亚铬酸铜催化剂.用得到的催化剂按下列流程进行实验(已知:浓硫酸在常温下不氧化NO气体).

根据题意完成下列各题:
(1)装置③可以选的干燥剂为:
A.浓硫酸 B.碱石灰 C.硅胶 D.无水氯化钙
(2)若实验室只提供浓氨水和生石灰两种试剂,你会选择下图

(3)若实验室提供稀硝酸、铜丝和小颗粒石灰石,若选用上图D装置制取较纯NO,其操作方法是:
(4)装置⑥中,小段玻璃管的作用是
(5)装置⑦的作用可能是:
(6)若进入装置⑤的NO共2688mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下2016mL N2,则NO的转化率为:
下列对于Na2O2的叙述中,正确的是( )
| A、Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物 | B、Na2O2能与水反应,所以Na2O2可以作气体干燥剂 | C、Na2O2与水反应时,Na2O2是氧化剂,水是还原剂 | D、Na2O2与二氧化碳反应时,Na2O2既是氧化剂又是还原剂 |