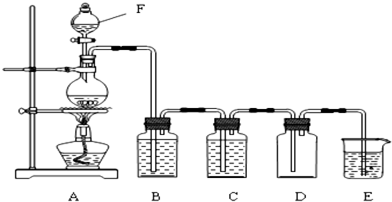
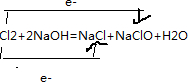摘要:14.画出实验室制取氯气的装置图(包括气体发生装置.气体进化装置.气体收集装置.尾气收集装置)
网址:http://m.1010jiajiao.com/timu3_id_209430[举报]
某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c、d表示止水夹).
(1)B是一种可以随开随制,随关随停的制备气体的装置.检验装置B的气密性方法 是 .
(2)上述 (填写序号)相连后的装置可用于制取和收集氯气.写出实验室制取氯气的化学方程式 .
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁的操作是 .
②试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满溶液,则NO2与通入O2的物质的量比为 .
查看习题详情和答案>>

(1)B是一种可以随开随制,随关随停的制备气体的装置.检验装置B的气密性方法 是
(2)上述
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹
②试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满溶液,则NO2与通入O2的物质的量比为
(Ⅰ)实验室制取氯气的装置如图:
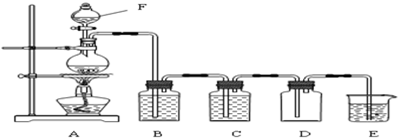
(1)仪器F的名称是 ;按图组装好装置后首先要进行的操作是: .
(2)装置B中盛放的试剂是 ,其作用是 ;装置E中盛放的试剂是 ,作用是 .
(3)写出E中发生反应的化学方程式: .
(Ⅱ)实验室也可以用浓盐酸与高锰酸钾反应来制取少量的氯气,反应的化学方程式为:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O
(1)该反应的氧化剂是 ,氧化产物是 .
(2)浓盐酸在反应中显示出来的性质是 (填编号).
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)若用足量的浓盐酸与一定量的二氧化锰反应,产生的氯气在标准状况下的体积为11.2L,则反应中被氧化的HCl的质量为多少?(要求计算过程) 查看习题详情和答案>>

(1)仪器F的名称是
(2)装置B中盛放的试剂是
(3)写出E中发生反应的化学方程式:
(Ⅱ)实验室也可以用浓盐酸与高锰酸钾反应来制取少量的氯气,反应的化学方程式为:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O
(1)该反应的氧化剂是
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)若用足量的浓盐酸与一定量的二氧化锰反应,产生的氯气在标准状况下的体积为11.2L,则反应中被氧化的HCl的质量为多少?(要求计算过程) 查看习题详情和答案>>
某化学兴趣小组为探究SO2的性质,按如图Ⅰ所示装置进行实验.


请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是 ;其中发生反应的化学方程式 .
(2)实验过程中,装置B、C中发生反应的现象分别是 、 ,这些现象分别说明SO2具有的性质是 和 ;
(3)该实验小组的甲、乙两位同学利用上述图Ⅱ装置继续进行实验:通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅.试根据该实验装置和两名同学的实验结果回答问题.
①请写出实验室制取氯气的化学方程式: ;
如何除去所制氯气中混有的氯化氢杂质: .
②试分析甲同学实验过程中,品红溶液不褪色的原因是(用离子方程式表示): .
③你认为乙同学是怎样做到让品红溶液变得越来越浅的? .
查看习题详情和答案>>


请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是
(2)实验过程中,装置B、C中发生反应的现象分别是
(3)该实验小组的甲、乙两位同学利用上述图Ⅱ装置继续进行实验:通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅.试根据该实验装置和两名同学的实验结果回答问题.
①请写出实验室制取氯气的化学方程式:
如何除去所制氯气中混有的氯化氢杂质:
②试分析甲同学实验过程中,品红溶液不褪色的原因是(用离子方程式表示):
③你认为乙同学是怎样做到让品红溶液变得越来越浅的?
图是实验室制取Cl2并以纯净、干燥的Cl2为原料进行特定反应的实验装置图: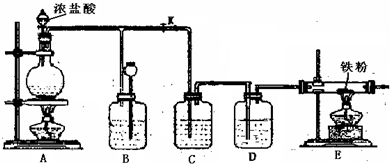
(1)写出实验室制取氯气的离子反应方程式:
(2)C中盛装的液体是
(3)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃E处的酒精灯.E装置内盛有铁粉,写出E装置中反应的化学方程式:
(4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是
(5)该装置的设计是否合理
查看习题详情和答案>>

(1)写出实验室制取氯气的离子反应方程式:
MnO2+4H++2Cl-(浓)
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-(浓)
Mn2++Cl2↑+2H2O
.
| ||
(2)C中盛装的液体是
饱和食盐水
饱和食盐水
,D中盛装的液体是浓硫酸
浓硫酸
.(3)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃E处的酒精灯.E装置内盛有铁粉,写出E装置中反应的化学方程式:
2Fe+3Cl2
2FeCl3
| ||
2Fe+3Cl2
2FeCl3
;
| ||
(4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是
B中液面下降,长颈漏斗内液面升高,B中液面上方有黄绿色气体;
B中液面下降,长颈漏斗内液面升高,B中液面上方有黄绿色气体;
,B的作用是可以使内压降低,充当储气瓶.
可以使内压降低,充当储气瓶.
.(5)该装置的设计是否合理
否
否
(填“是“或“否”),如果不合理,请加以改正或用NaOH溶液处理尾气
或用NaOH溶液处理尾气
.