摘要:将一定质量的Mg和Al的混合物投入足量稀硫酸中.固体全部溶解并产生气体.待反应完全后.向所得溶液中加入NaOH溶液.生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示. 请计算:(1)Mg和Al的质量分别是多少? (2)硫酸溶液的物质的量浓度是多少? 2009-2010学年度第一学期第三次调研考试 高一化学试卷 答案:1-5:C D C A B 6-10:C B B A D 11-15:D AC AD C D 16-20: BD C A D A 21-25: BD B A A C 26-30: BD AD A B C
网址:http://m.1010jiajiao.com/timu3_id_207122[举报]
 将一定质量的Mg和Al的混合物投入250mL、2.0mol/L稀硫酸中,固体全部溶解并产生气体0待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
将一定质量的Mg和Al的混合物投入250mL、2.0mol/L稀硫酸中,固体全部溶解并产生气体0待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
查看习题详情和答案>>
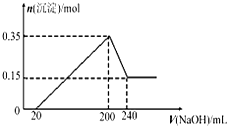 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示,则下列说法不正确的是( )
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示,则下列说法不正确的是( )| A、Mg和Al的总质量为9g | B、生成的H2在标准状况下的体积为11.2L | C、NaOH溶液的物质的量浓度为5mol/L | D、硫酸的物质的量浓度为1mol/L |
将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。

则下列说法正确的是( )
A.Mg和Al的总质量为
C.NaOH溶液的物质的量浓度为5 mol·L-1 D.生成的H2在标准状况下的体积为

