题目内容
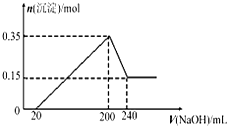
 将一定质量的Mg和Al的混合物投入250mL、2.0mol/L稀硫酸中,固体全部溶解并产生气体0待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
将一定质量的Mg和Al的混合物投入250mL、2.0mol/L稀硫酸中,固体全部溶解并产生气体0待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )分析:由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后硫酸有剩余,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O.当V(NaOH溶液)=200mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,二者物质的量之和为0.25mol,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(Na2SO4)等于200mL氢氧化钠溶液中含有的n(NaOH)的
倍.从200mL开始,NaOH溶解Al(OH)3:NaOH+Al(OH)3=NaAlO2+2H2O,当沉淀不再减少,此时全部为Mg(OH)2,物质的量为0.15mol,所以沉淀量最大时,Mg(OH)2为0.15mol,Al(OH)3为0.25mol-0.15mol=0.1mol,
A、铝离子水解,溶液呈酸性;
B、由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后硫酸有剩余,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O;
C、沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(NaOH)=2n(Na2SO4)据此计算;
D、由元素守恒可知n(Al)=n[Al(OH)3]=0.1mol,n(Mg)=n[Mg(OH)2]=0.15mol,根据电子转移守恒可知2n(H2)=3n(Al)+2n(Mg),据此计算n(H2),再根据V=nVm计算氢气体积.
| 1 |
| 2 |
A、铝离子水解,溶液呈酸性;
B、由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后硫酸有剩余,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O;
C、沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(NaOH)=2n(Na2SO4)据此计算;
D、由元素守恒可知n(Al)=n[Al(OH)3]=0.1mol,n(Mg)=n[Mg(OH)2]=0.15mol,根据电子转移守恒可知2n(H2)=3n(Al)+2n(Mg),据此计算n(H2),再根据V=nVm计算氢气体积.
解答:解:由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后硫酸有剩余,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O.当V(NaOH溶液)=200mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,二者物质的量之和为0.25mol,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(Na2SO4)等于200mL氢氧化钠溶液中含有的n(NaOH)的
倍.从200mL开始,NaOH溶解Al(OH)3:NaOH+Al(OH)3=NaAlO2+2H2O,当沉淀不再减少,此时全部为Mg(OH)2,物质的量为0.15mol,所以沉淀量最大时,Mg(OH)2为0.15mol,Al(OH)3为0.25mol-0.15mol=0.1mol,
A、溶质有硫酸镁、硫酸铝和硫酸钠,铝离子水解,溶液呈酸性,故A错误;
B、由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后硫酸有剩余,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O,溶质有硫酸镁、硫酸铝和硫酸钠,故B错误;
C、沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(NaOH)=2n(Na2SO4)=2×0.25L×2mol/L=1mol,所以Na0H溶液的物质的量浓度为
=5 mol/L,故C正确;
D、由元素守恒可知n(Al)=n[Al(OH)3]=0.1mol,n(Mg)=n[Mg(OH)2]=0.15mol,根据电子转移守恒可知2n(H2)=3n(Al)+2n(Mg),根据电子转移守恒可知2n(H2)=3n(Al)+2n(Mg)=3×0.1mol+2×0.15mol=0.6mol,所以n(H2)=0.3mol,故氢气体积为0.3mol×22.4mol/L=7.72L,故D错误;
故选C.
| 1 |
| 2 |
A、溶质有硫酸镁、硫酸铝和硫酸钠,铝离子水解,溶液呈酸性,故A错误;
B、由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后硫酸有剩余,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O,溶质有硫酸镁、硫酸铝和硫酸钠,故B错误;
C、沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(NaOH)=2n(Na2SO4)=2×0.25L×2mol/L=1mol,所以Na0H溶液的物质的量浓度为
| 1mol |
| 0.2L |
D、由元素守恒可知n(Al)=n[Al(OH)3]=0.1mol,n(Mg)=n[Mg(OH)2]=0.15mol,根据电子转移守恒可知2n(H2)=3n(Al)+2n(Mg),根据电子转移守恒可知2n(H2)=3n(Al)+2n(Mg)=3×0.1mol+2×0.15mol=0.6mol,所以n(H2)=0.3mol,故氢气体积为0.3mol×22.4mol/L=7.72L,故D错误;
故选C.
点评:本题考查镁铝的重要化合物、化学计算,以图象题的形式考查,题目难度中等,注意分析图象各阶段的物质的量的关系,根据各阶段的化学反应,利用守恒计算.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示,则下列说法不正确的是( )
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示,则下列说法不正确的是( )| A、Mg和Al的总质量为9g | B、生成的H2在标准状况下的体积为11.2L | C、NaOH溶液的物质的量浓度为5mol/L | D、硫酸的物质的量浓度为1mol/L |
 (2009?长春一模)将一定质量的Mg和Al的混合物投入1mol?L-1500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
(2009?长春一模)将一定质量的Mg和Al的混合物投入1mol?L-1500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( ) 将一定质量的Mg和Al混合物投入500mL 稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
将一定质量的Mg和Al混合物投入500mL 稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )