摘要:27. 实验室常用浓盐酸与二氧化锰反应来制取氯气.反应的化学方程式为 .现用密度为1.19g/cm3.质量分数为
网址:http://m.1010jiajiao.com/timu3_id_206397[举报]
实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O.
上述反应中MnO2发生
查看习题详情和答案>>
| ||
上述反应中MnO2发生
还原
还原
(填“氧化”或“还原”)反应,每有1molMnO2参加反应,转移2
2
mol电子.实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O.
(1)写出该反应的离子方程式
(2)在反应中MnO2发生
(3)当0.1mol MnO2参加反应时,转移电子数为
查看习题详情和答案>>
| ||
(1)写出该反应的离子方程式
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||
(2)在反应中MnO2发生
还原
还原
(填“氧化”或“还原”)反应,Cl2是氧化
氧化
(同上)产物.(3)当0.1mol MnO2参加反应时,转移电子数为
0.2NA
0.2NA
,被氧化的HCl为0.2
0.2
mol.实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
(1)如果上述反应使用的是质量分数为36.5%,密度为1.18g.cm-3的浓盐酸,则该盐酸的物质的量浓度是多少?(要求小数点后保留一位数字)
(2)如果反应产生的氯气在标准状况下的体积为11.2L,请计算参加反应的HCl的物质的量,以及反应中被氧化的HCl的物质的量.
查看习题详情和答案>>
| ||
(1)如果上述反应使用的是质量分数为36.5%,密度为1.18g.cm-3的浓盐酸,则该盐酸的物质的量浓度是多少?(要求小数点后保留一位数字)
(2)如果反应产生的氯气在标准状况下的体积为11.2L,请计算参加反应的HCl的物质的量,以及反应中被氧化的HCl的物质的量.
实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式如下:
MnO2+4HCl
MnCl2+Cl2↑+2H2O
(1)该反应属于氧化还原吗?如果是,指出其中的氧化剂和还原剂;如果不是,说明理由.
(2)密度为1.19g?cm-3、溶质的质量分数为36.5%的浓盐酸200mL,跟足量二氧化锰发生反应,产生的氯气在标准状况下的体积为11.2L.计算参加反应的浓盐酸的体积以及反应中被氧化的HCl的物质的量.
查看习题详情和答案>>
MnO2+4HCl
| ||
(1)该反应属于氧化还原吗?如果是,指出其中的氧化剂和还原剂;如果不是,说明理由.
(2)密度为1.19g?cm-3、溶质的质量分数为36.5%的浓盐酸200mL,跟足量二氧化锰发生反应,产生的氯气在标准状况下的体积为11.2L.计算参加反应的浓盐酸的体积以及反应中被氧化的HCl的物质的量.
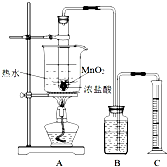 实验室常用浓盐酸与二氧化锰反应制取氯气.浓盐酸和二氧化锰反应过程中,浓盐酸的浓度不断降低,当盐酸浓度降至临界浓度时,反应停止.
实验室常用浓盐酸与二氧化锰反应制取氯气.浓盐酸和二氧化锰反应过程中,浓盐酸的浓度不断降低,当盐酸浓度降至临界浓度时,反应停止.方法一:
甲同学利用图装置,测定盐酸浓度降至临界浓度时 反应生成氯气的体积,来探究在某温度下浓盐酸与二氧化锰反应的临界浓度.
方法:A中试管有足量的MnO2,往其中加入10mol/L的浓盐酸,控制温度为80℃进行反应.甲同学进行了三次同样的实验,收集气体(体积均换算成标准状况),数据如下表:
| 第一次实验 | 第二次实验 | 第三次实验 | |
| 盐酸的用量 | 10.0mL | 10.0mL | 10.0mL |
| 氯气的体积 | 225mL | 192mL | 223mL |
(1)请写出A中试管内反应的离子方程式
(2)检验该装置的气密性的方法是
(3)B中加入的溶液为
(4)为计算与二氧化锰反应的浓盐酸临界浓度,甲同学的第
方法二:
(5)乙同学认为该实验有不足之处:浓盐酸易挥发,会造成上述所测的临界浓度
乙同学提出可直接用反应后A中的溶液来测定盐酸的临界浓度:
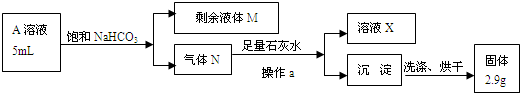
(6)以上图表中操作a的名称是
(7)请写出A溶液中的物质与NaHCO3溶液反应的离子方程式:
(8)根据以上数据,浓盐酸与二氧化锰制氯气的反应中浓盐酸的临界浓度为