网址:http://m.1010jiajiao.com/timu3_id_205891[举报]
钠的性质实验:
(1)钠的氧化:用________从试剂瓶中取出一小块钠,先将钠表面的煤油用滤纸吸干,然后再用小刀切割.可以观察到新切开的断面呈现________,很快此断面逐渐变暗,原因是________.(2)钠的燃烧:取一小块擦去煤油的金属钠,放在坩埚上加热,可以观察到钠的表面逐渐熔化,发出________火焰;燃烧后的固体产物呈________色,其成分是________.
(3)钠与水的反应:取切绿豆大小的钠粒,同时要将多余的钠块________.将切下的钠块投入盛有水的烧杯中(事先滴入几滴酚酞溶液),看到的现象可以概括为:“浮”、“熔”、“游”、“嘶”、“红”.对现象的相应解释是:钠的密度比水的小、钠与水反应放热且放出的热使具有较低熔点的钠熔化、生成的氢气推动钠在水面上四处游动、发生嘶嘶声至完全消失、钠与水反应生成了碱性物质——NaOH.
| 实验步骤 | 实验现象 |
| ①将一小块金属钠投入滴有酚酞试液的冷水中 | 钠块浮在水面上,熔化成闪亮的小球,做不定向移动,随之消失,溶液变红色 |
| ②将表面积大致相同的镁条和铝条(均已用砂纸打磨过)分别投入足量的相同体积0.5mol?L-1盐酸中 | 镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快 |
| ③将新制氯水滴加到新制的Na2S溶液中 | |
| ④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol?L-1盐酸和3mol?L-1盐酸中 | 剧烈反应产生气体,但铝粉消失比镁条快 |
(1)实验①中可以说明该反应是放热反应的现象是
(2)由实验②可得出决定化学反应快慢的主要因素是
(3)实验③的现象是产生浅黄色沉淀,离子方程式为
由实验③可以得出非金属性氯
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确?
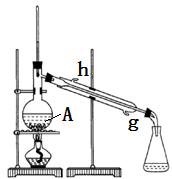
某化学小组采用如图装置,以冰醋酸和异戊醇制备少量乙酸异戊酯(俗称:香蕉水)。
已知:CH3COOH+HOCH2CH2CH(CH3)2  CH3COOCH2CH2CH(CH3)2+H2O
CH3COOCH2CH2CH(CH3)2+H2O
| | 密度(g/m L) L) | 熔点(℃) | 沸点(℃) | 溶解性 |
| 冰醋酸 | 1.049 | 16.6 | 118.1 | 能溶于水 |
| 异戊醇 | 0.812 | -117.2℃ | 130.5 | 微溶于水 |
| 乙酸异戊酯 | 0.869 | -78℃ | 140 | 难溶于水 |
(1)制备粗品
在50mL干燥的 中(填仪器名称)加入10mL(8.1g , 0.092mol)异戊醇和10mL(10.5g , 0.175mol)冰醋酸,振摇下缓缓加入2.5mL浓硫酸并使其混合均匀,再投入几块碎瓷片,装上冷凝管,冷却水从_________口进入,控制温度100℃左右,加热回流至锥形瓶中液体无明显增加为止。
A中碎瓷片的作用是
锥形瓶中的液体主要是 ,采用边反应边将其蒸出的方法的目的是 。
(2)制备精品
①反应结束后,冷却反应物至室温。将装置A中的反应混合物倒入分液漏斗中,用少量饱和食盐水荡洗反应瓶,一起并入分液漏斗。用饱和食盐水代替蒸馏水的优点是 。
②振摇分液漏斗,静置分层后分去水层。有机层先用25 mL 10% 碳酸钠水溶液洗涤除去 杂质 ,再用水洗涤两次。分尽水层后将酯层转入干燥的锥形瓶中,用 (填写选项)干燥0.5h。
a.五氧化二磷 b.碱石灰 c.无水硫酸镁 d.生石灰
③将干燥后的液体过滤到装置A中,加热蒸馏收集 ℃的馏分,称重,产物重8.4g,则该实验的产率为 。(保留两位有效数字)
 查看习题详情和答案>>
查看习题详情和答案>>
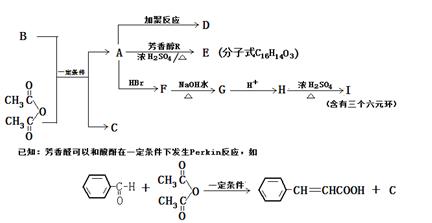
已知:CH3COOH+HOCH2CH2CH(CH3)2
 CH3COOCH2CH2CH(CH3)2+H2O
CH3COOCH2CH2CH(CH3)2+H2O| | 密度(g/m L) L) | 熔点(℃) | 沸点(℃) | 溶解性 |
| 冰醋酸 | 1.049 | 16.6 | 118.1 | 能溶于水 |
| 异戊醇 | 0.812 | -117.2℃ | 130.5 | 微溶于水 |
| 乙酸异戊酯 | 0.869 | -78℃ | 140 | 难溶于水 |
(1)制备粗品
在50mL干燥的 中(填仪器名称)加入10mL(8.1g , 0.092mol)异戊醇和10mL(10.5g , 0.175mol)冰醋酸,振摇下缓缓加入2.5mL浓硫酸并使其混合均匀,再投入几块碎瓷片,装上冷凝管,冷却水从_________口进入,控制温度100℃左右,加热回流至锥形瓶中液体无明显增加为止。
A中碎瓷片的作用是
锥形瓶中的液体主要是 ,采用边反应边将其蒸出的方法的目的是 。
(2)制备精品
①反应结束后,冷却反应物至室温。将装置A中的反应混合物倒入分液漏斗中,用少量饱和食盐水荡洗反应瓶,一起并入分液漏斗。用饱和食盐水代替蒸馏水的优点是 。
②振摇分液漏斗,静置分层后分去水层。有机层先用25 mL 10% 碳酸钠水溶液洗涤除去 杂质 ,再用水洗涤两次。分尽水层后将酯层转入干燥的锥形瓶中,用 (填写选项)干燥0.5h。
a.五氧化二磷 b.碱石灰 c.无水硫酸镁 d.生石灰
③将干燥后的液体过滤到装置A中,加热蒸馏收集 ℃的馏分,称重,产物重8.4g,则该实验的产率为 。(保留两位有效数字)
某化学小组采用如图装置,以冰醋酸和异戊醇制备少量乙酸异戊酯(俗称:香蕉水)。
已知:CH3COOH+HOCH2CH2CH(CH3)2 CH3COOCH2CH2CH(CH3)2+H2O
|
| 密度(g/mL) | 熔点(℃) | 沸点(℃) | 溶解性 |
| 冰醋酸 | 1.049 | 16.6 | 118.1 | 能溶于水 |
| 异戊醇 | 0.812 | -117.2℃ | 130.5 | 微溶于水 |
| 乙酸异戊酯 | 0.869 | -78℃ | 140 | 难溶于水 |
实验步骤:
(1)制备粗品
在50mL干燥的 中(填仪器名称)加入10mL(8.1g , 0.092mol)异戊醇和10mL(10.5g , 0.175mol)冰醋酸,振摇下缓缓加入2.5mL浓硫酸并使其混合均匀,再投入几块碎瓷片,装上冷凝管,冷却水从_________口进入,控制温度100℃左右,加热回流至锥形瓶中液体无明显增加为止。
A中碎瓷片的作用是
锥形瓶中的液体主要是 ,采用边反应边将其蒸出的方法的目的是 。
(2)制备精品
①反应结束后,冷却反应物至室温。将装置A中的反应混合物倒入分液漏斗中,用少量饱和食盐水荡洗反应瓶,一起并入分液漏斗。用饱和食盐水代替蒸馏水的优点是 。
②振摇分液漏斗,静置分层后分去水层。有机层先用25 mL 10% 碳酸钠水溶液洗涤除去 杂质 ,再用水洗涤两次。分尽水层后将酯层转入干燥的锥形瓶中,用 (填写选项)干燥0.5h。
a.五氧化二磷 b.碱石灰 c.无水硫酸镁 d.生石灰
③将干燥后的液体过滤到装置A中,加热蒸馏收集 ℃的馏分,称重,产物重8.4g,则该实验的产率为 。(保留两位有效数字)
查看习题详情和答案>>