摘要:4.A[说明]B中MnO4-有颜色.C中AlO2-不能存在.D中SiO32-不能存在.
网址:http://m.1010jiajiao.com/timu3_id_203312[举报]
(1)第ⅢA、ⅤA族元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似.Ga原子的电子排布式为 .在GaN晶体中,每个Ga原子与 个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为 .在四大晶体类型中,GaN属于 晶体.N元素原子的价层电子的轨道表示式为 .
(2)人工模拟酶是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合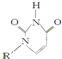 或C
或C
(Ⅰ)如下图(Ⅰ表示化合价为+1)时,分别形成a和b:
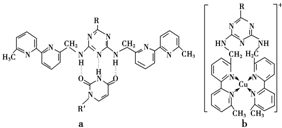
①a中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有 键的特性.
②C、N、H、O四种元素的电负性由小到大的顺序为 .C与O构成的常见的CO2的电子式为 .写出N与O形成和CO2的等电子体物质的化学式为 .
③微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用力的差异 .
(③a中微粒间相互作用为分子间氢键和范德华力,b中是配位键)
查看习题详情和答案>>
(2)人工模拟酶是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合
 或C
或C(Ⅰ)如下图(Ⅰ表示化合价为+1)时,分别形成a和b:

①a中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有
②C、N、H、O四种元素的电负性由小到大的顺序为
③微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用力的差异
(③a中微粒间相互作用为分子间氢键和范德华力,b中是配位键)
 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算.实验中加热至恒重的目的是
保证NaHCO3全部分解
保证NaHCO3全部分解
.(2)方案二:按图装置进行实验.并回答以下问题.
①实验前先
检查装置的气密性
检查装置的气密性
.分液漏斗中应该装硫酸
硫酸
(“盐酸”或“硫酸”).D装置的作用是
防止空气中水蒸气、CO2进入C管被吸收
防止空气中水蒸气、CO2进入C管被吸收
.②实验中除称量样品质量外,还需称
C
C
装置前后质量的变化.③根据此实验得到的数据,测定结果有误差.因为实验装置还存在一个明显缺陷,该缺陷是
装置A、B中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差
装置A、B中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差
.(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液.过滤洗涤,干燥沉淀,称量固体质量,计算:
①过滤操作中,除了烧杯,漏斗外,还用到的玻璃仪器有
玻璃棒
玻璃棒
.②实验中判断沉淀是否完全的方法是
取少量上层清液,滴加少量BaCl2溶液,如无白色沉淀说明沉淀完全
取少量上层清液,滴加少量BaCl2溶液,如无白色沉淀说明沉淀完全
.③已知称得样品21.2g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为
50%
50%
.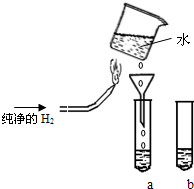 某实验探究小组进行氢气在空气中燃烧的实验探究,装置如图所示(固定装置略去),在试管a和b中分别装入少量下表溶液进行实验:
某实验探究小组进行氢气在空气中燃烧的实验探究,装置如图所示(固定装置略去),在试管a和b中分别装入少量下表溶液进行实验:| 实验 | 试管a | 试管b(作对比用) | 试管a中实验现象 |
| ① | KI-淀粉溶液 | KI-淀粉溶液 | 溶液变蓝色 |
| ② | 酸性高锰酸钾稀溶液 | 酸性高锰酸钾稀溶液 | 溶液紫红色褪去 |
| A、热水可使KI-淀粉溶液和酸性高锰酸钾溶液变色 |
| B、H2在空气中燃烧可能有H2O2生成 |
| C、用H2燃烧产生的热来加热水 |
| D、对燃烧产生的水进行过滤 |
 如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极.在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示.请回答下列问题:
如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹;x、y分别为直流电源的两极.在A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入一多孔的惰性电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,生成气体如图所示.请回答下列问题:(1)标出电源的正、负极:x为
正
正
.(2)在滤纸的C端附近,观察到的现象是
滤纸变蓝
滤纸变蓝
.?(3)写出电极反应式:B电极
4OH--4e=2H2O+O2↑
4OH--4e=2H2O+O2↑
.?(4)若电解一段时间后,A、B中均有气体包围电极.此时切断开关S2闭合开关S1,则电流计的指针是否发生偏转
偏转
偏转
(填“偏转”或“不偏转”).?(5)若电流计指针偏转,写出有关的电极反应(若指针“不偏转”,此题不必回答):
2H2+4OH--4e=4H2O,2H2O+O2+4e=4OH-
2H2+4OH--4e=4H2O,2H2O+O2+4e=4OH-
;若电流计指针不偏转,请说明理由(若指针“偏转”,此题不必回答)不填
不填
.以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选) .
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl→CH3CH2Cl+H2O
C.CH3CH3+Cl2
CH3CH2Cl+HCl
D.CH2=CHCl+H2
CH3CH2Cl
由上述四个反应可归纳出,原子经济性高的是 反应(填反应类型).
(2)有毒物质的无害化也是绿色化学研究的内容之一.ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性酸根离子氧化除去.请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式 ,并说明该方法的优点 .
(3)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:
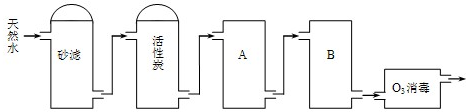
活性炭的作用是 ;O3消毒的优点是 .
A、B中放置的物质名称分别是:A B .
查看习题详情和答案>>
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选)
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl→CH3CH2Cl+H2O
C.CH3CH3+Cl2
| 光 |
D.CH2=CHCl+H2
| 催化剂 |
由上述四个反应可归纳出,原子经济性高的是
(2)有毒物质的无害化也是绿色化学研究的内容之一.ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性酸根离子氧化除去.请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式
(3)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:

活性炭的作用是
A、B中放置的物质名称分别是:A