摘要:5.D[说明] A中Fe2+会被酸性条件下的NO3-氧化.B中Ba2+与SO42-反应生成沉淀.C中I-会被酸性条件下的NO3-氧化.
网址:http://m.1010jiajiao.com/timu3_id_203277[举报]
(2010?南通模拟)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物.以孔雀石为原料可制备CuSO4?5H2O及纳米材料G,步骤如下:

已知:
请回答下列问题:
(1)溶液A中含有Cu2+、Fe2+、Fe3+.根据上述实验过程,可作为试剂①的最合理的是
a.KMnO4b.(NH4)2S c.H2O2 d.KSCN
(2)向溶液B中加入CuO的作用是
(3)由溶液C获得CuSO4?5H2O,需要经过
(4)制备纳米材料G时,应向CaCl2溶液中先通入
(5)欲测定溶液A中Fe2+的浓度,可取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,滴定时盛放待测液A的玻璃仪器是
查看习题详情和答案>>

已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.7 | 6.7 |
(1)溶液A中含有Cu2+、Fe2+、Fe3+.根据上述实验过程,可作为试剂①的最合理的是
c
c
(填代号).a.KMnO4b.(NH4)2S c.H2O2 d.KSCN
(2)向溶液B中加入CuO的作用是
调节溶液的pH,促进Fe3+的水解
调节溶液的pH,促进Fe3+的水解
.(3)由溶液C获得CuSO4?5H2O,需要经过
蒸发浓缩、冷却结晶、过滤
蒸发浓缩、冷却结晶、过滤
操作.(4)制备纳米材料G时,应向CaCl2溶液中先通入
NH3
NH3
(填化学式)写出该反应的化学方程式2NH3+CO2+CaCl2+H2O=CaCO3↓+2NH4Cl
2NH3+CO2+CaCl2+H2O=CaCO3↓+2NH4Cl
.(5)欲测定溶液A中Fe2+的浓度,可取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,滴定时盛放待测液A的玻璃仪器是
锥形瓶
锥形瓶
(填名称);滴定达到终点的现象为当滴入最后一滴KMnO4,溶液变成紫红色且半分钟内不褪色
当滴入最后一滴KMnO4,溶液变成紫红色且半分钟内不褪色
.孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4?5H2O及CaCO3,步骤如下:
试回答下列问题:

(1)在未加入H2O2的溶液A中,存在的金属离子有Cu2+、Fe2+、Fe3+.若检验该溶液中Fe3+,选择最合适的试剂是
A.KMnO4溶液 B.Fe粉 C. Na2CO3溶液 D.KSCN溶液
向溶液A中加入H2O2,H2O2在该反应中作氧化剂.实验室选用H2O2而不用Cl2作氧化剂.除考虑环保因素外,另一原因是不引入杂质
(2)由溶液C获得CuSO4?5H2O,需要经过加热浓缩,
(3)制备CaCO3时,发生反应的化学方程式是
(4)欲测定溶液A中Fe2+的浓度,需配制100mL 0.1mol∕LKMnO4标准溶液.配制该溶液时:除烧杯、玻璃棒、胶头滴管外,还需的一种玻璃仪器是
查看习题详情和答案>>
试回答下列问题:

(1)在未加入H2O2的溶液A中,存在的金属离子有Cu2+、Fe2+、Fe3+.若检验该溶液中Fe3+,选择最合适的试剂是
D
D
(填代号).A.KMnO4溶液 B.Fe粉 C. Na2CO3溶液 D.KSCN溶液
向溶液A中加入H2O2,H2O2在该反应中作氧化剂.实验室选用H2O2而不用Cl2作氧化剂.除考虑环保因素外,另一原因是不引入杂质
Cl-
Cl-
离子.(2)由溶液C获得CuSO4?5H2O,需要经过加热浓缩,
(冷却)结晶
(冷却)结晶
,过滤等操作.除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器,该仪器在此操作中的主要作用是引流
引流
.(3)制备CaCO3时,发生反应的化学方程式是
CO2+CaCl2+2NH3?H2O=CaCO3↓+2NH4Cl+H2O
CO2+CaCl2+2NH3?H2O=CaCO3↓+2NH4Cl+H2O
;若实验过程中有氨气逸出,可选用下列装置中的B
B
(填代号)装置吸收氨气.(4)欲测定溶液A中Fe2+的浓度,需配制100mL 0.1mol∕LKMnO4标准溶液.配制该溶液时:除烧杯、玻璃棒、胶头滴管外,还需的一种玻璃仪器是
100mL容量瓶
100mL容量瓶
;当往该玻璃仪器中加蒸馏水至接近刻度线1-2cm时,应改用胶头滴管
胶头滴管
滴加蒸馏水至溶液的凹液面正好与刻度线相平.(2012?大兴区一模)某学习小组为研究低价态氮元素物质的还原性,以NH3为例设计了如下图实验(夹持设备略去)

Ⅰ.检验气密性后关闭弹簧夹I打开弹簧夹Ⅱ,点燃酒精灯,铜丝红热后打开分液漏斗的活塞,A中气体进入B中时不断通入空气,反应一段时间后熄灭酒精灯.
Ⅱ.(1)能证明有氨气产生的现象是
 .
.
(2)C中铜丝在熄灭酒灯后仍保持红热说明其中反应为
(3)D中产生红棕色气体和白烟,产生白烟的化学方程式为:
(4)F中也产生大量白烟,写出该反应中反应物的物质的量之比n(NH3):n(Cl2)
(5)用化学方程式及相应理论说明A中能产生大量NH3气体的原因
(6)装置中A稍有不足,应该怎样改进
(7)C中铜丝可以与H2O2和H2SO4的混合溶液发生化学反应,已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)H=64.39KJ?mol-1
2H2O2(l)═2H2O(l)+O2(g)H=-196.46KJ?mol-1
H2(g)+
O2(g)═H2O(l)H=-285.84KJ?mol-1
写出在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式
查看习题详情和答案>>

Ⅰ.检验气密性后关闭弹簧夹I打开弹簧夹Ⅱ,点燃酒精灯,铜丝红热后打开分液漏斗的活塞,A中气体进入B中时不断通入空气,反应一段时间后熄灭酒精灯.
Ⅱ.(1)能证明有氨气产生的现象是
A中湿润的红色石蕊试纸变蓝
A中湿润的红色石蕊试纸变蓝
;氨分子电子式为

(2)C中铜丝在熄灭酒灯后仍保持红热说明其中反应为
放
放
热反应(填“吸热”或“放热”NH3在C中反应的化学方程式为4NH3+5O2
4NO+6H2O,2NH3+3CuO
3Cu+N2+3H2O
| ||
| △ |
| ||
| △ |
4NH3+5O2
4NO+6H2O,2NH3+3CuO
3Cu+N2+3H2O
.
| ||
| △ |
| ||
| △ |
(3)D中产生红棕色气体和白烟,产生白烟的化学方程式为:
HNO3+NH3=NH4NO3
HNO3+NH3=NH4NO3
(4)F中也产生大量白烟,写出该反应中反应物的物质的量之比n(NH3):n(Cl2)
8:3
8:3
(5)用化学方程式及相应理论说明A中能产生大量NH3气体的原因
NH3+H2O?NH3.H2O?NH4++OH-△H<0,氢氧化钠使c(OH-)增大,平衡逆向移动,同时氢氧化钠溶于水放出大量热,也使平衡逆向移动,产生大量氨气
NH3+H2O?NH3.H2O?NH4++OH-△H<0,氢氧化钠使c(OH-)增大,平衡逆向移动,同时氢氧化钠溶于水放出大量热,也使平衡逆向移动,产生大量氨气
,比较某时刻A中分液漏斗溶液平衡常数K1和三颈瓶中溶液的平衡常数K2大小关系,K1>
>
K2(填“<”“=”“>”).(6)装置中A稍有不足,应该怎样改进
装置中A装置分液漏斗与三颈瓶之间增加一气压平衡管
装置中A装置分液漏斗与三颈瓶之间增加一气压平衡管
.(7)C中铜丝可以与H2O2和H2SO4的混合溶液发生化学反应,已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)H=64.39KJ?mol-1
2H2O2(l)═2H2O(l)+O2(g)H=-196.46KJ?mol-1
H2(g)+
| 1 |
| 2 |
写出在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式
Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1
Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1
.孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物.实验室以孔雀石为原料制备CuSO4?5H2O及纳米材料G,步骤如图所示:
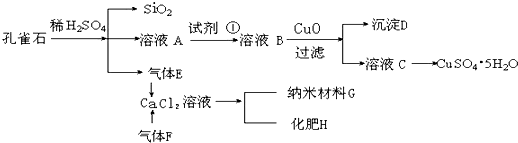
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+.从下列所给试剂中选择:实验步骤中试剂①最佳为
a.KMnO4/H+ b.Cl2 c.H2O2 d.KSCN
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为
(2)由溶液C获得CuSO4?5H2O,需要经过
(3)制备纳米材料G时,应向CaCl2溶液中选通入(或先加入)
(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4标准溶液应使用
查看习题详情和答案>>

请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+.从下列所给试剂中选择:实验步骤中试剂①最佳为
c
c
(填代号),检验溶液A中Fe3+的最佳试剂为d
d
(填代号).a.KMnO4/H+ b.Cl2 c.H2O2 d.KSCN
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为
Fe(OH)3
Fe(OH)3
,加入CuO作用是调节溶液pH值,使Fe3+的水解生成氢氧化铁沉淀而除去
调节溶液pH值,使Fe3+的水解生成氢氧化铁沉淀而除去
.(2)由溶液C获得CuSO4?5H2O,需要经过
蒸发、冷却结晶、过滤
蒸发、冷却结晶、过滤
操作.除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是引流
引流
.(3)制备纳米材料G时,应向CaCl2溶液中选通入(或先加入)
NH3
NH3
(填化学式).写出该反应的化学方程式2NH3+CO2+CaCl2+H2O=CaCO3+2NH4Cl
2NH3+CO2+CaCl2+H2O=CaCO3+2NH4Cl
.(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4标准溶液应使用
酸式滴定管
酸式滴定管
.取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,终点现象为溶液变成紫红色并保持半分钟内不褪色
溶液变成紫红色并保持半分钟内不褪色
.(2009?山东)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4?5H2O及CaCO3,步骤如下:

请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+:从下列所给试剂中选择:实验步骤中试剂①为0
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4?5H2O,需要经过加热蒸发,
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应
查看习题详情和答案>>

请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+:从下列所给试剂中选择:实验步骤中试剂①为0
c
c
(填代号),检验溶液A中Fe3+的最佳试剂为d
d
(填代号).a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4?5H2O,需要经过加热蒸发,
冷却结晶
冷却结晶
,过滤等操作.除烧杯、漏斗外,过滤操作还用到另一玻璃仪器玻璃棒
玻璃棒
,该仪器在此操作中的主要作用是搅拌、引流
搅拌、引流
.(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)
NH3?H2O
NH3?H2O
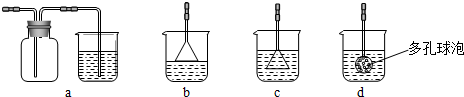
(填化学式).若实验过程中有氨气逸出、应选用下列b
b
装置回收(填代号).
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应
与刻度线相平
与刻度线相平
,直到溶液凹液面最低处与刻度线相切
溶液凹液面最低处与刻度线相切
.用KMnO4标准溶液滴定时应选用酸式
酸式
滴定管(填“酸式”或“碱式”).