网址:http://m.1010jiajiao.com/timu3_id_202906[举报]
B. 50 mL 0.05 mol/L的MgCl2溶液
C. 50 mL 0.2 mol/L的HCl溶液
D. 100 mL 0.2 mol/L的KCl溶液
|
与100 mL 0.1 mol/L的NaCl溶液中Cl-离子浓度相同的是 | |
| [ ] | |
A. |
50 mL 0.2 mol/L的NaCl溶液 |
B. |
50 mL 0.05 mol/L的MgCl2溶液 |
C. |
50 mL 0.2 mol/L的HCl溶液 |
D. |
100 mL 0.2 mol/L的KCl溶液 |
海水中蕴藏着丰富的资源,海水综合利用的流程图如下.

(1)用NaCl做原料可以得到多种产品.
①工业上由NaCl制备金属钠的化学方程式是________.
②实验室用惰性电极电解100 mL 0.1 mol/L NaCl溶液,若阴阳两极均得到112 mL气体(标准状况),则所得溶液的pH为________(忽略反应前后溶液的体积变化).
③电解氯化钠稀溶液可制备“84消毒液”,通电时产生的氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:________.
(2)分离出粗盐后的卤水中蕴含丰富的镁资源,经转化后可获得MgCl2粗产品.
①粗产品的溶液中含有Na+、Fe3+、Fe2+和Mn2+,需将Fe3+、Fe2+、Mn2+转化为沉淀除去;Fe(OH)2呈絮状,常将其转化为Fe(OH)3而除去(生成氢氧化物沉淀的pH见表).若只加入题(1)中得到的一种产品即可达到上述除杂目的,则该产品的化学式为________,最终控制溶液的pH值为________.
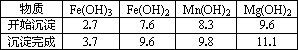
②在家用电热水器不锈钢内胆表面镶嵌镁棒,利用电化学原理来防止内胆腐蚀,写出正极的电极反应式:________.
(3)碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在.几种粒子之间有如下转化关系:
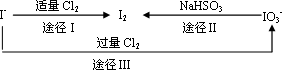
①如以途径Ⅰ制取I2,加的Cl2要适量,如过量就会发生途径Ⅲ的副反应,在该副反应产物中,IO3-与Cl-物质的量之比为1∶6,则氧化剂和还原剂物质的量之比为________.
②如以途径Ⅱ在溶液中制取I2,反应后的溶液显酸性,则反应的离子方程式是
________
(10分) 利用所学化学反应原理,解决以下问题:
(1)某溶液含两种相同物质的量的溶质,溶液中只存在OH—、H+、NH4+、Cl-四种离子,且c(NH4+)>c(Cl-)>c(OH—)>c(H+),则这两种溶质是 _________ 。
(2)0.1 mol·L-1的氨水与0.05 mol·L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性: 。
(3)以石墨电极电解100 mL 0.1 mol·L-1CuSO4溶液。若阳极上产生气体的物质的量为0.01 mol,则阴极上析出Cu的质量为 g。
(4)将AgCl分别放入①5mL H2O ②10mL0.2mol·L-1 MgCl2 ③20 mL0.5mol·L-1 NaCl溶液 ④40 mL0.1mol·L-1HCl中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是________________。
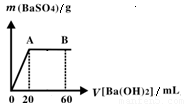
(5)向20 mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如右图所示,B点溶液的pH=7(忽略溶液体积变化),则c(HCl)=_________mol·L-1。
查看习题详情和答案>>
(1)某溶液含两种相同物质的量的溶质,溶液中只存在OH—、H+、NH4+、Cl-四种离子,且c(NH4+)>c(Cl-)>c(OH—)>c(H+),则这两种溶质是 _________ 。
(2)0.1 mol·L-1的氨水与0.05 mol·L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性: 。
(3)以石墨电极电解100 mL 0.1 mol·L-1CuSO4溶液。若阳极上产生气体的物质的量为0.01 mol,则阴极上析出Cu的质量为 g。
(4)将AgCl分别放入①5mL H2O ②10mL0.2mol·L-1 MgCl2③20 mL0.5mol·L-1 NaCl溶液④40 mL0.1mol·L-1HCl中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是________________。
(5)向20 mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如右图所示,B点溶液的pH=7(忽略溶液体积变化),则c(HCl)=_________mol·L-1。
