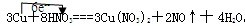摘要:20.已知铜在常温下能被HN03溶解.反应方程式为: (1)请将上述反应改成离子方程式 . (2)上述反应中.氧化剂是 .氧化产物是--.没有全部参加氧化还原反应.没有参加氧化还原反应的硝酸占参加反应的全部硝酸的 .
网址:http://m.1010jiajiao.com/timu3_id_201765[举报]
已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目)
(2)上述反应中氧化剂是
(3)当生成0.5mol的 NO时,反应转移电子是
查看习题详情和答案>>
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目)
(2)上述反应中氧化剂是
HNO3
HNO3
,氧化产物是Cu(NO3)2
Cu(NO3)2
.(3)当生成0.5mol的 NO时,反应转移电子是
1.5
1.5
mol,同时还原的硝酸为31.5
31.5
克.已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3══3Cu(NO3)2+2NO↑+4H2O
(1)用单线桥法分析上述反应.
(2)上述反应的离子方程式为
查看习题详情和答案>>
(1)用单线桥法分析上述反应.
(2)上述反应的离子方程式为
3Cu+8H++2NO3-══3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-══3Cu2++2NO↑+4H2O
,还原产物是NO
NO
(填化学式). 标况下生成3.36L NO,被还原的硝酸的物质的量为0.15mol
0.15mol
.已知铜在常温下能被稀硝酸溶解,反应方程式为:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
(1)用单线桥法标出电子得失的方向和数目

(2)上述反应中氧化剂是
.
查看习题详情和答案>>
(1)用单线桥法标出电子得失的方向和数目


(2)上述反应中氧化剂是
HNO3
HNO3
,氧化产物是Cu(NO3)2
Cu(NO3)2
.没有参加氧化还原反应的硝酸占总硝酸的| 3 |
| 4 |
| 3 |
| 4 |