摘要:22.与100mL 0.1mol·L-1 Na2SO4溶液中含有的Na+数目相同的是( ) A.0.1mol·L-1NaNO3溶液50mL B.0.2mol·L-1NaOH溶液100mL C.0.2mol·L-1 NaCl溶液50mL D.0.1mol·L-1 Na2CO3溶液100mL
网址:http://m.1010jiajiao.com/timu3_id_200919[举报]
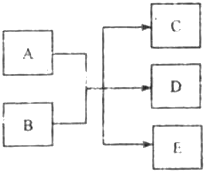 (2011?河西区一模)在一定条件下,物质A~E相互转化的关系如下图所示,其中A为单质,常温下E是无色液体.请根据条件回答下列问题(填写化学用语):
(2011?河西区一模)在一定条件下,物质A~E相互转化的关系如下图所示,其中A为单质,常温下E是无色液体.请根据条件回答下列问题(填写化学用语):(1)若A、C、D中均含有氯元素,其中氯的化合价由低到高的顺序为C、A、D.C为氯碱工业的原料,D的溶液有漂白性.则D的电子式为


Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
;(2)若B为短周期某种元素X的最高价氧化物的水化物.
①若A为亮红色固体,在加热条件下能与B的浓溶液反应,但不能与B的稀溶液反应,则元素x在周期表中的位置是
第三周期第ⅥA族
第三周期第ⅥA族
:若在常温下A与B的浓、稀溶液均能反应,则A与B的稀溶液反应的高于方程式是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
.②若A为黑色固体,在加热条件下与B的浓溶液反应产生两种无色气体,则此反应的化学方程式是
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.
| ||
(3)已知(1)中的B溶液电离出的阴离子M与(2)中的B溶液电离出的阳离子N都是10电子粒子,当100mL 0.5mol/L的M与100mL 0.55mol/LN完全反应生成E时放出akJ热量,该反应的热化学方程式为
H3O+(aq)+OH-(aq)=2H2O(l)△H=-20akJ/mol
H3O+(aq)+OH-(aq)=2H2O(l)△H=-20akJ/mol
.室温下,下列各选项中所述的两个量,前者一定大于后者的是( )
| A、pH=10的NaOH和Na2CO3溶液中,水的电离程度 | B、将pH=3的盐酸和醋酸分别稀释成pH=5的溶液,需加水的体积 | C、10mL0.1 mol?L-1的醋酸与100mL 0.01 mol?L-1的醋酸中的H+物质的量 | D、物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中NH4+的物质的量浓度 |