摘要:2.用容量瓶配制一定物质的量浓度的溶液.该容量瓶必须是 ( ) A.干燥的 B.用欲配的溶液润洗过的 C.瓶塞不漏水 D.以上三项均须要求的
网址:http://m.1010jiajiao.com/timu3_id_198599[举报]
(2013?临沂三模)工业上利用某合金废料(含铁、铜、碳)为原料制备CuSO4和(NH4)2SO4?FeSO4?6H2O(莫尔盐)的工艺流程如下:

回答下列问题:
(1)实验室用容量瓶配制一定物质的量浓度的稀硫酸,定容时若俯视刻度线,则会导致配制的溶液浓度
(2)步骤②和步骤③中会产生同一种气体,生成该气体的离子方程式为:
(3)用Cu和混酸(稀硫酸、稀硝酸)制备CuSO4溶液时,为得到纯净的CuSO4溶液,混酸中硫酸和硝酸的浓度之比最好为
(4)浓度均为0.1mol?L-1的莫尔盐溶液和(NH4)2SO4溶液中,c(NH4+)前者大于后者,原因是
(5)莫尔盐比绿矾(FeSO4?7H2O)更稳定,常用于定量分析.利用莫尔盐溶液可将酸性KMnO4还原为Mn2+,反应的离子方程式为:
(6)某化学兴趣小组设计用如图所示装置制备(NH4)2SO4溶液.
①装置A圆底烧瓶中的固体试剂为
②将装置B中两种液体分离开,所需的最主要的玻璃仪器为
③装置C的作用为
查看习题详情和答案>>

回答下列问题:
(1)实验室用容量瓶配制一定物质的量浓度的稀硫酸,定容时若俯视刻度线,则会导致配制的溶液浓度
偏大
偏大
(填“偏大”、“偏小”或“无影响”).(2)步骤②和步骤③中会产生同一种气体,生成该气体的离子方程式为:
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
.(3)用Cu和混酸(稀硫酸、稀硝酸)制备CuSO4溶液时,为得到纯净的CuSO4溶液,混酸中硫酸和硝酸的浓度之比最好为
3:2
3:2
.(4)浓度均为0.1mol?L-1的莫尔盐溶液和(NH4)2SO4溶液中,c(NH4+)前者大于后者,原因是
莫尔盐溶液中Fe2+的水解显酸性,抑制了NH4+的水解
莫尔盐溶液中Fe2+的水解显酸性,抑制了NH4+的水解
.(5)莫尔盐比绿矾(FeSO4?7H2O)更稳定,常用于定量分析.利用莫尔盐溶液可将酸性KMnO4还原为Mn2+,反应的离子方程式为:
5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O
5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O
.(6)某化学兴趣小组设计用如图所示装置制备(NH4)2SO4溶液.
①装置A圆底烧瓶中的固体试剂为
生石灰或氢氧化钠、碱石灰等
生石灰或氢氧化钠、碱石灰等
(填试剂名称).②将装置B中两种液体分离开,所需的最主要的玻璃仪器为
分液漏斗
分液漏斗
(填仪器名称).③装置C的作用为
吸收尾气,防止氨气污染空气
吸收尾气,防止氨气污染空气
.实验:
(1)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: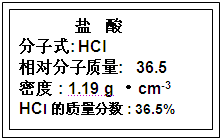
①该浓盐酸中HCl的物质的量浓度为
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D溶液的密度
(2)实验室配制480mL0.08mol/LNa2CO3溶液回答下列问题
①应用托盘天平称取十水碳酸钠晶体
②若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是
③用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
A、干燥的 B、瓶塞不漏水 C、用欲配制的溶液润洗过 D、以上三项都要求
④若实验遇下列情况,溶液的浓度是“偏高”、“偏低”还是“不变”?
A.加水时越过刻度线
B.忘记将洗涤液加入容量瓶
C.容量瓶内壁附有水珠而未干燥处理
D.溶解后没有冷却便进行定容
(3)①取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为
②取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为
③在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL FeCl3饱和溶液,继续煮沸至溶液呈
④另取一小烧杯加入25mL蒸馏水后,向烧杯中再加入2mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到
查看习题详情和答案>>
(1)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

①该浓盐酸中HCl的物质的量浓度为
11.9
11.9
mol?L-1.②取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是BD
BD
.A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D溶液的密度
(2)实验室配制480mL0.08mol/LNa2CO3溶液回答下列问题
①应用托盘天平称取十水碳酸钠晶体
11.4
11.4
g②若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是
10.6
10.6
g(1g以下用游码)③用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
B
B
A、干燥的 B、瓶塞不漏水 C、用欲配制的溶液润洗过 D、以上三项都要求
④若实验遇下列情况,溶液的浓度是“偏高”、“偏低”还是“不变”?
A.加水时越过刻度线
偏低
偏低
;B.忘记将洗涤液加入容量瓶
偏低
偏低
;C.容量瓶内壁附有水珠而未干燥处理
不变
不变
;D.溶解后没有冷却便进行定容
偏高
偏高
.(3)①取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为
Fe2O3+6H+=2Fe3++3H2O
Fe2O3+6H+=2Fe3++3H2O
,反应后得到黄色的FeCl3溶液.用此溶液做以下实验:②取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为
Fe3++3O H-=Fe(OH)3↓
Fe3++3O H-=Fe(OH)3↓
.③在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中加入2mL FeCl3饱和溶液,继续煮沸至溶液呈
红褐
红褐
色,即可制得Fe(OH)3胶体.④另取一小烧杯加入25mL蒸馏水后,向烧杯中再加入2mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到
乙
乙
(填甲或乙)烧杯中会产生丁达尔效应.此实验可以区别溶液和胶体
溶液和胶体
.用容量瓶配制一定物质的量浓度的NaCl溶液的实验中,会使所配溶液浓度偏高的是( )
| A、定容时加水加多了,用滴管吸出溶液至刻度线 | B、定容时俯视刻度线 | C、没有洗涤溶解NaCl固体的烧杯和玻璃棒 | D、称量NaCl固体时砝码上有杂质 |