摘要:23.下图中①-⑪分别代表有关反应物中的一种物质.请填写以下空白. (1)①.②.⑤.⑩的化学式分别是 . . . , (2)③与④反应的化学方程式是 ; (3)⑦与⑪反应的化学方程式是 ; (4)⑧与⑨反应的化学方程式是 .
网址:http://m.1010jiajiao.com/timu3_id_198116[举报]
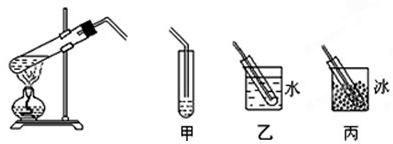
101.3kPa下,溴乙烷、乙酸、乙酸乙酯的沸点分别为38.2℃、117.9℃、77.1℃.在实验室里,制取少量的以上三种物质均可用下图中的发生装置.回答下列问题:
收集
收集
查看习题详情和答案>>

收集
乙酸乙酯
乙酸乙酯
时,使用甲装置,甲中所装试剂为饱和碳酸钠
饱和碳酸钠
;收集
乙酸
乙酸
时,使用乙装置;收集溴乙烷
溴乙烷
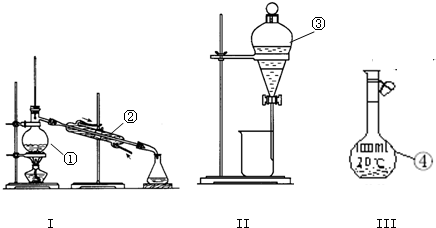
时,使用丙装置.(1)写出下图中序号①~④仪器的名称:
①
(2)仪器①~④中,使用时必须检查是否漏水的是
装置I、II、III中需要检查气密性是
(3)分离碘水中的碘应先选择装置
(4)现欲用98%的浓硫酸(密度为1.84g?cm-3)配制成浓度为1.0mol?L-1的稀硫酸100mL.
①所需仪器除烧杯、玻璃棒外还需
②所取浓硫酸的体积为
查看习题详情和答案>>

①
蒸馏烧瓶
蒸馏烧瓶
; ②冷凝管
冷凝管
; ③分液漏斗
分液漏斗
; ④100mL容量瓶;
100mL容量瓶;
;(2)仪器①~④中,使用时必须检查是否漏水的是
③④
③④
.(填仪器序号)装置I、II、III中需要检查气密性是
蒸馏装置
蒸馏装置
.(填装置名称)(3)分离碘水中的碘应先选择装置
II
II
(填装置序号)进行萃取
萃取
和分液
分液
操作,再用装置I
I
(填装置序号)进行蒸馏
蒸馏
操作.(4)现欲用98%的浓硫酸(密度为1.84g?cm-3)配制成浓度为1.0mol?L-1的稀硫酸100mL.
①所需仪器除烧杯、玻璃棒外还需
10mL量筒
10mL量筒
、100mL容量瓶
100mL容量瓶
、胶头滴管
胶头滴管
.②所取浓硫酸的体积为
5.4
5.4
mL.(保留一位小数)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁“.请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁“.实验中必须使用普通铁粉和6摩/升盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).填写下列空白:

(1)实验进行时试管A中应加入的试剂是
(2)实验时,U型管G中应加入的试剂是
(3)两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母)
(4)烧瓶I中发生的反应有时要加入少量硫酸铜溶液,其目的是
(5)试管E中发生反应的化学方程式是
(6)为了安全,在E管中的反应发生前,在F出口处必须
查看习题详情和答案>>

(1)实验进行时试管A中应加入的试剂是
普通铁粉(或铁粉)
普通铁粉(或铁粉)
;烧瓶B的作用是作为水蒸气发生器(或用来产生水蒸气)
作为水蒸气发生器(或用来产生水蒸气)
;烧瓶C的作用是防止水倒吸(或用作安全瓶)
防止水倒吸(或用作安全瓶)
;在试管D中收集得到的是氢气
氢气
.(2)实验时,U型管G中应加入的试剂是
固体NaOH(或碱石灰、CaO等碱性固体干燥剂)
固体NaOH(或碱石灰、CaO等碱性固体干燥剂)
;长颈漏斗H中应加入6摩/升的稀盐酸
6摩/升的稀盐酸
.(3)两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母)
A、B、E
A、B、E
.(4)烧瓶I中发生的反应有时要加入少量硫酸铜溶液,其目的是
加快氢气产生的速度
加快氢气产生的速度
.(5)试管E中发生反应的化学方程式是
Fe3O4+4H2
3Fe+4H2O
| ||
Fe3O4+4H2
3Fe+4H2O
.
| ||
(6)为了安全,在E管中的反应发生前,在F出口处必须
检验氢气的纯度
检验氢气的纯度
;E管中的反应开始后,在F出口处应点燃氢气
点燃氢气
.