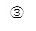题目内容
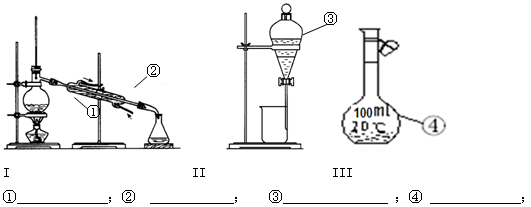
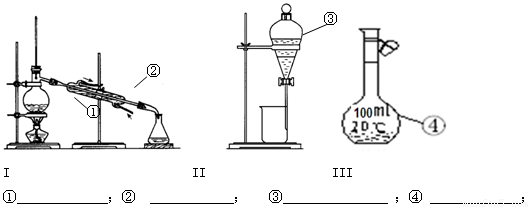
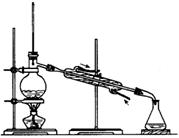
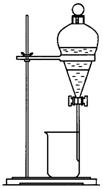
(1)写出下图中序号①~④仪器的名称:
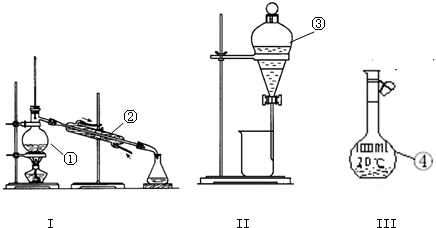
①
(2)仪器①~④中,使用时必须检查是否漏水的是
装置I、II、III中需要检查气密性是
(3)分离碘水中的碘应先选择装置
(4)现欲用98%的浓硫酸(密度为1.84g?cm-3)配制成浓度为1.0mol?L-1的稀硫酸100mL.
①所需仪器除烧杯、玻璃棒外还需
②所取浓硫酸的体积为

①
蒸馏烧瓶
蒸馏烧瓶
; ②冷凝管
冷凝管
; ③分液漏斗
分液漏斗
; ④100mL容量瓶;
100mL容量瓶;
;(2)仪器①~④中,使用时必须检查是否漏水的是
③④
③④
.(填仪器序号)装置I、II、III中需要检查气密性是
蒸馏装置
蒸馏装置
.(填装置名称)(3)分离碘水中的碘应先选择装置
II
II
(填装置序号)进行萃取
萃取
和分液
分液
操作,再用装置I
I
(填装置序号)进行蒸馏
蒸馏
操作.(4)现欲用98%的浓硫酸(密度为1.84g?cm-3)配制成浓度为1.0mol?L-1的稀硫酸100mL.
①所需仪器除烧杯、玻璃棒外还需
10mL量筒
10mL量筒
、100mL容量瓶
100mL容量瓶
、胶头滴管
胶头滴管
.②所取浓硫酸的体积为
5.4
5.4
mL.(保留一位小数)分析:(1)根据常见仪器的名称来回答;
(2)根据分液漏斗和100mL容量瓶在使用前要检查是否漏水;
根据产生气体的装置需检查气密性,分液漏斗和100mL容量瓶在使用前要检查是否漏水;
(3)萃取利用溶质在不同溶剂中溶解度不同,用一种溶剂把溶质从它与另一溶剂所组成的溶液中提取出来,然后分液;根据碘与四氯化碳的沸点不同可用蒸馏分离;
(4)①根据配制一定物质的量浓度溶液的步骤:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,确定需要的仪器;
②根据稀释前后溶质的质量不变来计算出溶液的体积.
(2)根据分液漏斗和100mL容量瓶在使用前要检查是否漏水;
根据产生气体的装置需检查气密性,分液漏斗和100mL容量瓶在使用前要检查是否漏水;
(3)萃取利用溶质在不同溶剂中溶解度不同,用一种溶剂把溶质从它与另一溶剂所组成的溶液中提取出来,然后分液;根据碘与四氯化碳的沸点不同可用蒸馏分离;
(4)①根据配制一定物质的量浓度溶液的步骤:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,确定需要的仪器;
②根据稀释前后溶质的质量不变来计算出溶液的体积.
解答:解:(1)因①~④仪器的名称分别为:蒸馏烧瓶、冷凝管、分液漏斗、100mL容量瓶,
故答案为:蒸馏烧瓶;冷凝管;分液漏斗;100mL容量瓶;
(2)因分液漏斗和100mL容量瓶在使用前要检查是否漏水,蒸馏烧瓶、冷凝管不需要检查是否漏水,因蒸馏装置,加热时产生气体,故需检查气密性,分液装置中和100mL容量瓶在使用前要检查是否漏水,
故答案为:③④;蒸馏装置;
(3)碘在四氯化碳中的溶解度较在水中大,并且四氯化碳和水互不相溶,可用萃取的方法分离,接着可用分液方法将两层液体分开;四氯化碳易挥发,可用蒸馏的方法分馏得到四氯化碳,
故答案为:II;萃取;分液;I;蒸馏;
(4)①配制顺序是:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,一般用量筒量取(用到胶头滴管)称量,在烧杯中稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以仪器除烧杯、玻璃棒还需10mL量筒、100mL容量瓶、胶头滴管,故答案为:10mL量筒;100mL容量瓶;胶头滴管;
②设需要98%H2SO4的体积为VmL,根据溶液稀释前后溶质质量不变则,VmL×1.84g/cm3×98%=100mL×1.0mol?L-1×98g/mol,解得V=5.4ml,所以溶液的体积为5.4ml,故答案为:5.4;
故答案为:蒸馏烧瓶;冷凝管;分液漏斗;100mL容量瓶;
(2)因分液漏斗和100mL容量瓶在使用前要检查是否漏水,蒸馏烧瓶、冷凝管不需要检查是否漏水,因蒸馏装置,加热时产生气体,故需检查气密性,分液装置中和100mL容量瓶在使用前要检查是否漏水,
故答案为:③④;蒸馏装置;
(3)碘在四氯化碳中的溶解度较在水中大,并且四氯化碳和水互不相溶,可用萃取的方法分离,接着可用分液方法将两层液体分开;四氯化碳易挥发,可用蒸馏的方法分馏得到四氯化碳,
故答案为:II;萃取;分液;I;蒸馏;
(4)①配制顺序是:计算→量取→稀释、冷却→移液→定容→摇匀→装瓶→贴签,一般用量筒量取(用到胶头滴管)称量,在烧杯中稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以仪器除烧杯、玻璃棒还需10mL量筒、100mL容量瓶、胶头滴管,故答案为:10mL量筒;100mL容量瓶;胶头滴管;
②设需要98%H2SO4的体积为VmL,根据溶液稀释前后溶质质量不变则,VmL×1.84g/cm3×98%=100mL×1.0mol?L-1×98g/mol,解得V=5.4ml,所以溶液的体积为5.4ml,故答案为:5.4;
点评:本题主要考查了常见仪器的用途、一定物质的量浓度溶液的配制,题目难度不大,注意不同分离提纯方法的适用对象以及操作原理,在配制一定物质的量浓度溶液时抓住步骤是找出实验所需仪器的关键.

练习册系列答案
相关题目