摘要:21.在一烧杯中盛有100gBaCl2和HCl 的混合溶液.向其中逐渐滴加溶质质 量分数为10%的Na2CO3溶液.混合溶 液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示: 请根据题意回答问题小问应有必要的计算): (1)在实验过程中.有气体放出.还可以看到的明显实验现象是 . (2)在实验过程中放出气体的总质量为 g. (3)当滴入Na2CO3溶液至图中B点时.通过计算求此所得不饱和溶液中溶质质量分数是多少? 四川省南充高中09-10年高一上学期入学考试
网址:http://m.1010jiajiao.com/timu3_id_197206[举报]
 (1)在一烧杯中盛有稀H2SO4 溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,(如图).向该烧杯里缓缓注入与稀H2SO4 等密度的Ba(OH)2 溶液至恰好完全反应.则在此实验过程中:①烧杯里观察到的现象为
(1)在一烧杯中盛有稀H2SO4 溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,(如图).向该烧杯里缓缓注入与稀H2SO4 等密度的Ba(OH)2 溶液至恰好完全反应.则在此实验过程中:①烧杯里观察到的现象为溶液里有白色沉淀产生,小球下沉到烧杯底
溶液里有白色沉淀产生,小球下沉到烧杯底
②写出反应的离子方程式2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
(2)如图所示a、b、c、d分别是几种常见漏斗的上半部,A、B、C、D是实际操作中各漏斗的下半部插入容器中的示意图,请指出A、B、C、D分别与a、b、c、d相匹配的组合及其组合后装置在实验中的应用,例如:C和a组合,用于制取气体.
①A与
c
c
组合,用于制取气体
制取气体
,②B与b
b
组合,用于分液
分液
,③B与
d
d
组合,用于过滤
过滤
,④D与d
d
组合,用于添加酒精
添加酒精
. (2010?中山模拟)如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应(设H2SO4和Ba(OH)2溶液密度相同).试回答:
(2010?中山模拟)如图所示,在一烧杯中盛有H2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央,向该烧杯中缓缓注入 Ba(OH)2溶液至恰好完全反应(设H2SO4和Ba(OH)2溶液密度相同).试回答:(1)此实验中,观察到的现象有:
①
溶液里有白色沉淀产生
溶液里有白色沉淀产生
;②小球下沉到烧杯底
小球下沉到烧杯底
.(2)写出实验过程中反应的离子方程式为
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
.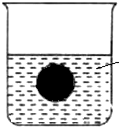 如图所示,在一烧杯中盛有100mlH2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央.向该烧杯里缓缓注入Ba(OH)2溶液至恰好完全反应,在此过程中:
如图所示,在一烧杯中盛有100mlH2SO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央.向该烧杯里缓缓注入Ba(OH)2溶液至恰好完全反应,在此过程中:(1)烧杯里观察到的实验现象有:①
产生白色沉淀
产生白色沉淀
②小球下沉至烧杯底部
小球下沉至烧杯底部
(2)写出实验过程中反应的离子方程式:
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
. 在一烧杯中盛有稀硫酸,有一塑料小球(与酸、碱均不发生反应)悬浮于溶液中,如图所示.
在一烧杯中盛有稀硫酸,有一塑料小球(与酸、碱均不发生反应)悬浮于溶液中,如图所示.(1)向烧杯中慢慢加入与稀硫酸密度相同(均大于1g?cm-3)的Ba(OH)2溶液至恰好反应完全,在实验中可观察到的现象有:
①
产生白色沉淀
产生白色沉淀
;②
小球下沉至烧杯底部
小球下沉至烧杯底部
.烧杯中所发生反应的离子方程式为
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
.(2)若向烧杯中加入的不是Ba(OH)2溶液,而是锌粒,在实验中可观察到的现象有:
①
有气泡冒出
有气泡冒出
;②
小球上浮
小球上浮
.烧杯中发生反应的离子方程式为
Zn+2H+=Zn2++H2↑
Zn+2H+=Zn2++H2↑
.
 _______________________________
_______________________________