网址:http://m.1010jiajiao.com/timu3_id_196929[举报]
(答题时,化学式及化学方程式中的M、E均用所对应的元素符号表示):
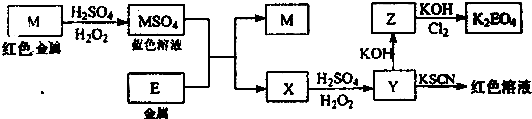
(1)写出M溶于稀H2SO4和H2O2混合液的离子方程式
(2)检验X中阳离子的方法和现象是
(3)某同学取X的溶液在空气中放置后,酸化并加入KI和淀粉溶液,溶液变为蓝色.试用离子方程式表示溶液变为蓝色的原因:
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、烧杯、玻璃棒、漏斗、铁架台外,还需要用到的硅酸盐仪器有
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图.A中试剂是盐酸.
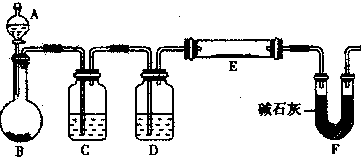
①装置D的作用
②连接好装置并检验装置的气密性后,应首先“加热反应管E”还是“从A瓶中逐滴加入液体”?
③该实验设计是否还有不足之处?若有请指出并改进,如没有本问可不答.
(6)试说明K2EO4可用作高效净水剂的原因
下图是牙膏中某些主要成分检验流程图,请回答以下问题:

(1)牙膏中的摩擦剂约占牙膏成分的50%,主要用于增强牙膏的摩擦作用和去污效果,不同种类的牙膏含有的摩擦剂有所不同,在上述流程图的第③步加入盐酸后会产生不同现象,请你填空:
摩擦剂 | 实验中出现的现象 | 解 释 |
SiO2 |
|
|
CaCO3 |
|
|
Ca3(PO4)2 | 溶解无气体,加NaOH至过量后又产生沉淀 |
|
Al(OH)3 | 溶解无气体,加NaOH至过量先产生沉淀后溶解 |
|
(2)日常生活中使用的牙膏里面都含有一定量的摩擦剂,试回答下列相关问题:
A.根据你的推测,摩擦剂应具备下列性质中的哪几条?
① 易溶于水 ②难溶于水 ③坚硬 ④柔软 ⑤颗粒较大 ⑥颗粒较小
B.据调查,两面针儿童牙膏、珍珠王防臭牙膏和中华透明牙膏中所使用的摩擦剂依次是氢氧化铝、碳酸钙和二氧化硅,它们所属的物质类别依次是 、 、 。
C.作牙膏摩擦剂的粉末状碳酸钙可以用石灰石来制备。以下是一种制备碳酸钙的生产方案,其流程图为,请你写出上述方案中有关反应的化学方程式:
(3)新制Cu(OH)2的配制方法是 。
牙膏中含有一定量的甘油,其主要功能是作保湿剂,在流程图的第②步得到的澄清溶液中加入新制Cu(OH)2,产生的现象是 ,化学方程式为
(4)实验测定澄清溶液的PH>7,可能原因是 。
(5)牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
Ca5(PO4)3OH(固) 5Ca2++3PO43-+OH-
进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是
已知Ca5(PO4)3F(固)的溶解度比上面的矿化产物更小,质地更坚固。主动脉用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋齿的原因:
根据以上原理,请你提出一种其它促进矿化的方法:
查看习题详情和答案>>