摘要:16.在探究铁.铜.锌.银的金属活动性顺序时.某小组做了如下三个实验:(所用金属的形状与大小及稀盐酸的用量均相同) (1)实验①中的反应化学方程式为 . (2)一段时间后.根据实验②观察到现象.可得出结论是 . (3)乙同学认为上述三个实验不能够得出四种金属的活动性顺序.还需要利用右图所示的实验装置.补充实验来实现探究目的.乙同学实验用的金属X是 .溶液Y是 ,. (4)丙同学用100g上述实验的盐酸分别跟足量的铁和锌反应.并绘制了生成氢气的物质的量的关系图.试回答: ① 判断甲.乙两图能表示丙同学所做实验结果是 图. ② 若用100g盐酸与足量的铁反应能生成0.2mol氢气.那么: (Ⅰ)该盐酸溶液含HCl物质的量是 . (Ⅱ)该盐酸的质量分数是 .
网址:http://m.1010jiajiao.com/timu3_id_19592[举报]
(2013?吉林一模)我们的日常生活离不开金属.
(1)铁生锈是铁与空气中的水蒸气、
(2)在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
①一段时间后,可观察到实验Ⅱ的现象是
②小组中的甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱.你认为他依据的实验现象是
③乙和丙两位同学认为上述三个实验不能够得出四种金属的活动性顺序,原因是
并在上述实验的基础上,补充了一个实验(图2所示),实现了探究目的.他们的实验:X是金属

查看习题详情和答案>>
(1)铁生锈是铁与空气中的水蒸气、
氧气
氧气
等发生化学反应的过程.(2)在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
①一段时间后,可观察到实验Ⅱ的现象是
红色固体表面有银白色固体析出,无色溶液变蓝色
红色固体表面有银白色固体析出,无色溶液变蓝色
;反应的化学方程式是Cu+2AgNO3═Cu(NO3)2+2Ag
Cu+2AgNO3═Cu(NO3)2+2Ag
②小组中的甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱.你认为他依据的实验现象是
实验Ⅲ中产生气体的速率比实验Ⅰ的快
实验Ⅲ中产生气体的速率比实验Ⅰ的快
.③乙和丙两位同学认为上述三个实验不能够得出四种金属的活动性顺序,原因是
无法比较Fe和Cu的活动性
无法比较Fe和Cu的活动性
;并在上述实验的基础上,补充了一个实验(图2所示),实现了探究目的.他们的实验:X是金属
Fe
Fe
,Y是CuSO4
CuSO4
溶液(写出化学式).
 29、我们的日常生活离不开金属.
29、我们的日常生活离不开金属.(1)右图是金属的一个应用实例,请说出利用了金属的什么物理性质?
导电性
(答出一点即可)延展性
.(2)据有关资料报导,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%-40%.铁生锈是铁与空气中的水蒸气、
氧气
等发生化学反应的过程.(3)在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
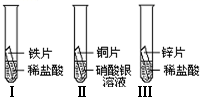
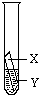 ①一段时间后,可观察到实验Ⅱ的现象是
①一段时间后,可观察到实验Ⅱ的现象是铜片表面有银白色固体附着
;反应的化学方程式是Cu+2AgNO3═Cu(NO3)2+2Ag
②小组中的甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱.你认为他依据的实验现象是
实验Ⅲ中产生气体的速度比实验Ⅰ的快
.③乙和丙两位同学认为上述三个实验不能够得出四种金属的活动性顺序,原因是
无法比较Fe和Cu的活动性
;并在上述实验的基础上,补充了一个实验(右图所示),实现了探究目的.他们的实验:X是金属
Fe
,Y是CuSO4
溶液(写出化学式).
在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如图所示三个实验:(所用金属的形状与大小及稀盐酸的用量均相同)
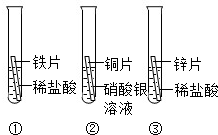
(1)实验①中的反应化学方程式为 .
(2)一段时间后,根据实验②观察到现象,可得出结论是 .
(3)乙同学认为上述三个实验不能够得出四种金属的活动性顺序,还需要利用如图所示的实验装置,补充实验来实现探究目的.
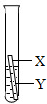
乙同学实验用的金属X是 ,溶液Y是 ;(其他合理答案也可)(要求写出化学式).
(4)丙同学用100g上述实验的盐酸分别跟足量的铁和锌反应,并绘制了生成氢气的质量(m/g)与时间(t/s)的关系图(如图所示).试回答:
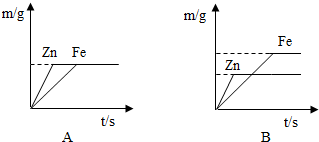
①判断A、B两图能表示丙同学所做实验结果是 图.
②若用100g盐酸与足量的铁反应能生成0.4g氢气.那么:
(Ⅰ)该盐酸溶液含HCl质量是 .
(Ⅱ)该盐酸中溶质的质量分数是 .
查看习题详情和答案>>

(1)实验①中的反应化学方程式为
(2)一段时间后,根据实验②观察到现象,可得出结论是
(3)乙同学认为上述三个实验不能够得出四种金属的活动性顺序,还需要利用如图所示的实验装置,补充实验来实现探究目的.

乙同学实验用的金属X是
(4)丙同学用100g上述实验的盐酸分别跟足量的铁和锌反应,并绘制了生成氢气的质量(m/g)与时间(t/s)的关系图(如图所示).试回答:

①判断A、B两图能表示丙同学所做实验结果是
②若用100g盐酸与足量的铁反应能生成0.4g氢气.那么:
(Ⅰ)该盐酸溶液含HCl质量是
(Ⅱ)该盐酸中溶质的质量分数是
21、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小及稀盐酸的质量分数和用量均相同)
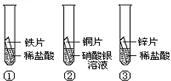
(1)实验①中的反应化学方程式为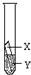
(2)一段时间后,根据实验②观察到现象,可得出结论是
(3)乙同学认为上述三个实验不能够得出四种金属的活动性顺序,还需要利用右图所示的实验装置,补充实验来实现探究目的.
乙同学实验用的金属X是
查看习题详情和答案>>

(1)实验①中的反应化学方程式为
Fe+2HCl=FeCl2+H2↑
.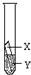
(2)一段时间后,根据实验②观察到现象,可得出结论是
铜的活泼性大于银
.(3)乙同学认为上述三个实验不能够得出四种金属的活动性顺序,还需要利用右图所示的实验装置,补充实验来实现探究目的.
乙同学实验用的金属X是
Fe
,溶液Y是
CuSO4(答案合理即可)
;(要求写出化学式). 在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)①一段时间后,可观察到实验Ⅱ现象是
铜片表面有银白色固体析出,溶液由无色变为蓝色
铜片表面有银白色固体析出,溶液由无色变为蓝色
;反应的化学方程式是Cu+2AgNO3═2Ag+Cu(NO3)2
Cu+2AgNO3═2Ag+Cu(NO3)2
;②甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁金属活动性强弱.你认为他依据的实验现象是
锌与酸反应的程度要比铁的剧烈
锌与酸反应的程度要比铁的剧烈
.③乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是
无法比较铁与铜的活动性
无法比较铁与铜的活动性
;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的.他们的实验:X是金属
Fe
Fe
,Y是CuSO4
CuSO4
溶液(写出化学式).