网址:http://m.1010jiajiao.com/timu3_id_195753[举报]
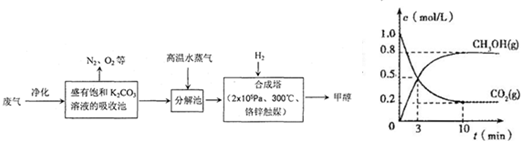
(1)合成塔中反应的化学方程式为
| 一定条件 |
| 一定条件 |
(2)从合成塔分离出甲醇的原理与下列
A.过滤 B.分液 C.蒸馏 D.结晶
(3)工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施.“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括
(4)在体积为2L的合成塔中,充入2mol CO2和6mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.从反应开始到平衡,v(H2)=
(5)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.3kJ/mol,H2 (g)+
| 1 |
| 2 |
 根据要求回答下列叙述相关问题
根据要求回答下列叙述相关问题Ⅰ、(1)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是
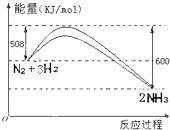
(2)如图是N2与H2反应过程中能量变化的曲线图.该反应的热化学方程式为:
根据此反应特点判断2molN2与足量的H2反应放出的热量
Ⅱ、已知CH4在O2中燃烧有如下两种反应途径
①CH4(g)+
| 3 |
| 2 |
②CO(g)+
| 1 |
| 2 |
③CH4(g)+2O2(g)→CO2(g)+2H2O (l)△H3
(1)根据盖斯定律写出上述物质转变过程中△H1、△H2、△H3的关系式
(2)比较|△H1|、|△H3|的大小是:|△H1|
碳及其含碳化合物在人们的生产生活中应用广泛。
(1)天然气是人们日常生活中的清洁能源。
已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l); △H1=-890.3kJ·mol-1
②2 CO(g)+O2(g)=2CO2 (g); △H2=-566 kJ·mol-1
则反应2 CH4(g)+3O2(g)=2CO(g)+4H2O(l)的△H=_____________。
(2)甲烷燃料电池的化学方程式为CH4+2O2=CO2+2H2O。某甲烷燃料电池以甲烷为燃料,以空气为氧化剂,以熔融的K2CO3(其中不含O2-和HCO3—)为电解质,以具有催化作用和导电性能的稀土金属为电极。
该燃料电池的负极电极反应式为:CH4-8e-+4CO32—=5CO2+2H2O,则其正极电极反应式为____________;为使电解质的组成保持稳定,使该燃料电池长时间稳定运行,在通入的空气中必须加入________________物质。
(3)以该燃料电池为电源,以铂作电极电解1000g 4.55%的NaOH溶液,一段时间后,溶液中溶质的质量分数变为5.00%,则阳极产生的气体在标准状况下的体积为________L。
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如下三组数据:
①实验A中以v(H2)表示的反应速率为___________________。
②通过计算可知,CO的转化率实验A_______________实验B(填“大于”、“等于”或“小于”),该反应的正反应为______________热反应(填“吸”或“放”)。
③若实验C要达到与实验B相同的平衡状态,则a、b应满足的关系是_________________(用含a、b的数学式表示)。
查看习题详情和答案>>
 2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式
。
2NH3的能量变化如图所示,写出生成氨气时该反应的热化学方程式
。
