网址:http://m.1010jiajiao.com/timu3_id_195430[举报]
|
用20 g NaOH配成250 mL溶液,从中取出5 mL,溶液物质的量浓度为: | |
| [ ] | |
A. |
0.02 mol/L |
B. |
0.01 mol |
C. |
1 mol/L |
D. |
2 mol/L |
某同学用标准NaOH溶液来测定未知浓度的盐酸的浓度:
(1)配制250 mL 0.5 mol/L的NaOH溶液所需的玻璃仪器为________.
(2)用滴定管准确量取20.00 mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用NaOH溶液滴定到终点.
该同学进行了三次实验,实验数据如下表:
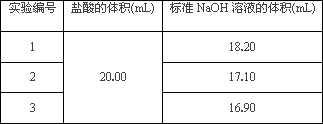
滴定中误差较大的是第________次实验,造成这种误差的可能原因是________(填选项编号)
a、在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
b、滴定管在盛装标准NaOH溶液前未润洗
c、滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
d、滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
e、滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f、达到滴定终点时,俯视溶液凹液面最低点读数
g、滴定到终点时,溶液颜色由无色变到了红色
(3)该同学所测得盐酸的物质的量浓度为________(结果保留三位小数).
A.在250 mL的容量瓶中定容,配制成250 mL烧碱溶液;
B.用碱式滴定管移取25 mL烧碱溶液于锥形瓶中,并滴几滴甲基橙指示剂;
C.在天平上准确称取烧碱样品20.5 g,在烧杯中用蒸馏水溶解;
D.将物质的量浓度为1.00 mol·L-1的标准硫酸溶液装入酸式滴定管中,调节液面,记下开始时的读数;
E.在锥形瓶下垫一张白纸,滴定至溶液变为橙色为止,记下读数。
试填空:
(1)正确操作步骤的顺序是(用字母填空)______→_______→_______→_______→_______。
(2)观察滴定管液面的读数时应注意什么问题?______________________________________。
(3)E步操作中的锥形瓶下垫一张白纸的作用是______________________。
(4)下列操作中可能使所测NaOH的质量分数偏低的是__________。
a.A步操作中未将溶液冷却至室温就转移到容量瓶中定容
b.C步操作中,称量药品时,砝码放在左盘,NaOH放在右盘
c.D步操作中酸式滴定管在装入标准H2SO4溶液前未用标准液润洗
d.读取硫酸体积时,开始时仰视读数,结束时俯视读数
(5)硫酸的初读数和末读数如图所示。末读数为________mL,初读数为_______mL,用量为
_______mL。按滴定所得数据来计算出的烧碱样品中NaOH的质量分数为__________。

草酸(H2C2O4)是一种易溶于水的二元中强酸,在水中它的存在形态有H2C2O4、HC2O![]() 、C2O
、C2O![]() ,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:
,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:

(1)图中曲线1表示________的分布系数变化;曲线3表示________的分布系数变化.
现有物质的量浓度均为0.1 mol/L的下列溶液:
①Na2C2O4
②NaHC2O4
③H2C2O4
④(NH4)2C2O4
⑤NH4HC2O4
已知NaHC2O4溶液显酸性.
(2)Na2C2O4溶液中,c(Na+)/c(C2O![]() )________2(填“>”、“=”、“<”),原因是________(用离子方程式表示).
)________2(填“>”、“=”、“<”),原因是________(用离子方程式表示).
(3)常温下,向10 mL 0.1 mol/L H2C2O4溶液中滴加0.1 mol/L NaOH溶液,随着NaOH溶液体积的增加,当溶液中c(Na+)=2c(C2O![]() )+c(HC2O
)+c(HC2O![]() )时,溶液显________性(填“酸”、“碱”或“中”),且V(NaOH)________10 mL(填“>”、“=”或“<”).
)时,溶液显________性(填“酸”、“碱”或“中”),且V(NaOH)________10 mL(填“>”、“=”或“<”).
(4)下列关于五种溶液的说法中,正确的是
A.
溶液②中,c(C2OB.
溶液②中,c(H2C2O4)+c(OH-)=c(C2OC.溶液④⑤中都符合c(NH![]() )+c(H+)=c(HC2O
)+c(H+)=c(HC2O![]() )+2c(C2O
)+2c(C2O![]() )+c(OH-)
)+c(OH-)
D.五种溶液都符合c(H2C2O4)+c(HC2O![]() )+c(C2O
)+c(C2O![]() )=0.1 mol·L-1.
)=0.1 mol·L-1.
(5)五种溶液中c(H2C2O4)
由大到小排列的顺序是________.(6)
配平氧化还原反应方程式:![]()
(7)
称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液.量取两份此溶液各25 mL,分别置于两个锥形瓶中.第一份溶液中加入2滴酚酞试液,滴加0.25 mol/L NaOH溶液至20 mL时,溶液由无色变为浅红色.第二份溶液用0.10 mol/L酸性KMnO4溶液滴定,滴定终点如何判断________.当加入16 mL 0.10 mol/L酸性KMnO4溶液时恰好反应完全.则原试样中H2C2O4·2H2O的质量分数为________,KHC2O4的质量分数为________.如果用0.25 mol/L NaOH溶液滴定第一份溶液的实验滴定终点仰视读数则测得的KHC2O4的质量分数________(填“偏高”“偏低”或“无影响”)为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0 g试样,加水溶解,配成250 mL试样溶液。
②用酸式滴定管量取25.00 mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500 mol/L NaOH溶液滴定,消耗NaOH溶液20.00 mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL。
回答下列问题:
(1)已知:0.10 mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为 。
(2)步骤①所需要的玻璃仪器有烧杯、玻璃棒、 。
(3)完成并配平下列离子方程式: C2O42-+ MnO4-+ H+= CO2+ Mn2++
(4)滴定时边滴边摇动锥形瓶,眼睛应观察 。
(5)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数 。(填“偏大”、“偏小”或“无影响”)
(6)步骤③中判断滴定终点的方法是 。
(7)试样中H2C2O4·2H2O的质量分数为 。
查看习题详情和答案>>