摘要:36].设计一种实验证明在酸性条件下.S2O82-的氧化性比MnO4-.Cr2O72-的强.MnO4-.Cr2O72-的氧化性比H2O2的强.写出相应反应的化学方程式.
网址:http://m.1010jiajiao.com/timu3_id_194067[举报]
金属钠、钙等在氧气中燃烧可生成过氧化物.从组成上分析,过氧化物为金属氧化物,可能会与水、二氧化碳、二氧化硫反应生成盐.
(1)取一支小试管,向其中加入过氧化纳固体,然后加入少量蒸馏水,将带余烬的小木条插入试管中,观察到的现象是
(2)有两个实验小组的同学用如图所示的装置进行实验,来探究过氧化钠与二氧化硫的反应
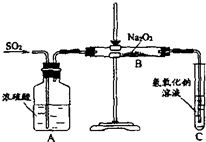
请回答下列问题:
①装置C中氢氧化钠溶液的作用是
②甲组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是:
③乙组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:
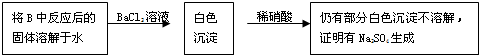
上述方案是否合理?
(3)为了解决养金鱼的吸氧问题,可在水中加入过氧化钙.某过氧化钠样品2.0g,加入到足量的水中,在标准状况下生成了224mL氧气.试计算该样品中含过氧化钙的质量分数.
查看习题详情和答案>>
(1)取一支小试管,向其中加入过氧化纳固体,然后加入少量蒸馏水,将带余烬的小木条插入试管中,观察到的现象是
有气体放出,小木条复燃
有气体放出,小木条复燃
,反应后,向其中滴入酚酞溶液,观察到的现象是溶液变红
溶液变红
.该反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(2)有两个实验小组的同学用如图所示的装置进行实验,来探究过氧化钠与二氧化硫的反应

请回答下列问题:
①装置C中氢氧化钠溶液的作用是
吸收二氧化硫气体
吸收二氧化硫气体
②甲组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是:
2Na2O2+2SO2=4Na2SO3+O2↑
2Na2O2+2SO2=4Na2SO3+O2↑
请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3.取白色固体,加入稀硫酸,产生能使品红溶液褪色的气体
取白色固体,加入稀硫酸,产生能使品红溶液褪色的气体
③乙组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:

上述方案是否合理?
不合理
不合理
.请简要说明两点理由:①稀硝酸能使亚硫酸钡转化为硫酸钡
稀硝酸能使亚硫酸钡转化为硫酸钡
;②若反应后残留过氧化钠,它溶于水后能将SO32-转化为SO42-
若反应后残留过氧化钠,它溶于水后能将SO32-转化为SO42-
.(3)为了解决养金鱼的吸氧问题,可在水中加入过氧化钙.某过氧化钠样品2.0g,加入到足量的水中,在标准状况下生成了224mL氧气.试计算该样品中含过氧化钙的质量分数.
 (2010?南宁二模)某化学兴趣小组在按图1装置做钠在空气中燃烧的实验时,观察到产物不仅仅有淡黄色的固体生成,还有少量的黑色颗粒产生,该小组对黑色颗粒进行了如下探究:
(2010?南宁二模)某化学兴趣小组在按图1装置做钠在空气中燃烧的实验时,观察到产物不仅仅有淡黄色的固体生成,还有少量的黑色颗粒产生,该小组对黑色颗粒进行了如下探究:(1)甲同学查阅资料知:钠与二氧化碳反应生成一种钠的正盐和一种黑色颗粒.据此推测黑色颗粒是
炭黑
炭黑
.写出生成该黑色颗粒的化学方程式:4Na+3CO2
2Na2CO3+C
| ||
4Na+3CO2
2Na2CO3+C
.
| ||
(2)乙同学认为只要将上述实验稍作改进,即可证明甲同学的猜想是否合理,请在图2的方框中画出装置图并注明相关药品的名称.
(3)丙同学按照乙同学的实验方案进行实验后,仍发现微量的黑色固体,于是认为可能是金属钠含有其它杂质,他发现在保存钠的试剂瓶的标签上有如下内容:
| 元素符号:Na纯度:89% 相对原子质量:22.99 磷酸盐-0.001% 硫酸盐-0.002% 铁-0.002% |
| 实验步骤 | 实验现象及结论 |
| ①收集上述微量黑色固体于试管中, 滴加过量的稀硫酸 滴加过量的稀硫酸 ②取少量反应后的溶液于试管中,滴加KSCN溶液 取少量反应后的溶液于试管中,滴加KSCN溶液 |
炭黑和铁的氧化物
炭黑和铁的氧化物
(填名称).有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验.通入SO2气体,将带火星的木条插入试管C中,木条复燃.请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3.
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:上述方案是否合理?
查看习题详情和答案>>

(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是
2Na2O2+2SO2═2Na2SO3+O2
2Na2O2+2SO2═2Na2SO3+O2
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3.
取白色固体,加稀硫酸,产生能使品红溶液褪色的气体
取白色固体,加稀硫酸,产生能使品红溶液褪色的气体
.(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:上述方案是否合理?
不合理
不合理
.请简要说明两点理由:①稀硝酸能将亚硫酸钡氧化为硫酸钡
稀硝酸能将亚硫酸钡氧化为硫酸钡
;②如果反应后的固体中还残留Na2O2也可将亚硫酸钡氧化为硫酸钡.
如果反应后的固体中还残留Na2O2也可将亚硫酸钡氧化为硫酸钡.
.
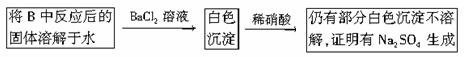 ?
?