网址:http://m.1010jiajiao.com/timu3_id_192897[举报]

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从碘水中分离出I2,选择装置
(3)装置A中①的名称是
(4)装置B在分液时为使液体顺利下滴,应进行的具体操作是
A.应该先将分液漏斗上的活塞拿下后再打开旋塞放出液体
B.加热
C.使分液漏斗上的活塞上的凹槽对准分液漏斗上的小孔后再打开旋塞放出液体.
Ⅱ.某同学按下列步骤配制250mL 0.2mol?L-1NaCl溶液,请回答有关问题.
| 实验步骤 | 有关问题 |
| ①计算所需NaCl的质量 | |
| ②称量NaCl固体 | 用托盘天平需要称量NaCl的质量为 2.9 2.9 g. |
| ③将NaCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施: 用玻璃棒搅拌 用玻璃棒搅拌 . |
| ④将烧杯中溶液转移至250mL容量瓶中 | 为了防止溶液溅出,应采取什么措施: 用玻璃棒引流 用玻璃棒引流 . |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1-2厘米处应如何操作: 改用胶头滴管加水至刻度线 改用胶头滴管加水至刻度线 . |
(2)取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需
(4)配制NaCl溶液时,下列操作情况会使结果偏高的是
A.移液前,容量瓶中有少量蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶瓶颈刻度线
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容.
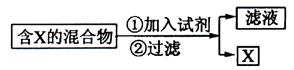
(Ⅰ)混合物的分离与提纯在化学实验中占有重要的位置。下图表示从固体混合物中分离X的方案,请回答有关问题。
![]() (1)
(1)
若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是 ,有关反应的化学方程式为 ;
![]() (2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作) 。
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作) 。
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(1)该工艺的中间过程会发生反应: ,反应的氧化剂是______________,氧化产物为__________
,反应的氧化剂是______________,氧化产物为__________
(2)在精炼铜的过程中,电解液中![]() 逐渐下降,
逐渐下降,![]() 、
、![]() 会逐渐增加,所以需定时除去其中的
会逐渐增加,所以需定时除去其中的![]() 、
、![]() 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。
| 物质 |
|
|
|
|
| 溶度积 |
|
|
|
|
甲同学设计了如下除杂方案:
![]()
①试剂a是__________,其目的是____________________________________;根据溶度积该方案能够除去的杂质金属阳离子是____________。写出检验该杂质金属阳离子的操作方法:____________________________________________________________________________.
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使![]() 生成
生成![]() 。沉淀而除去。”乙同学认为甲同学的方案中也
。沉淀而除去。”乙同学认为甲同学的方案中也
应该将溶液pH调至7~8。你认为乙同学的建议是否正确?________(填“是”或“否”),
理由是________________________________________________________________________。
查看习题详情和答案>>(14分)(Ⅰ)混合物的分离与提纯在化学实验中占有重要的位置。下图表示从固体混合物中分离X的方案,请回答有关问题。
(1)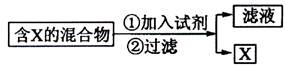
若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是 ,有关反应的化学方程式为 ;
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作) 。
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(1)该工艺的中间过程会发生反应: ,反应的氧化剂是______________,氧化产物为__________
,反应的氧化剂是______________,氧化产物为__________
(2)在精炼铜的过程中,电解液中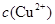 逐渐下降,
逐渐下降,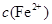 、
、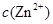 会逐渐增加,所以需定时除去其中的
会逐渐增加,所以需定时除去其中的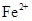 、
、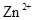 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。
| 物质 |  | 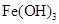 | 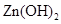 |  |
溶度积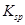 | 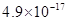 | 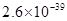 | 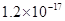 | 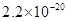 |
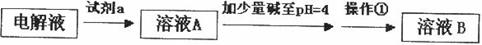
①试剂a是__________,其目的是____________________________________;根据溶度积该方案能够除去的杂质金属阳离子是____________。写出检验该杂质金属阳离子的操作方法:____________________________________________________________________________.
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使
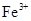 生成
生成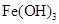 。沉淀而除去。”乙同学认为甲同学的方案中也
。沉淀而除去。”乙同学认为甲同学的方案中也应该将溶液pH调至7~8。你认为乙同学的建议是否正确?________(填“是”或“否”),
理由是________________________________________________________________________。 查看习题详情和答案>>
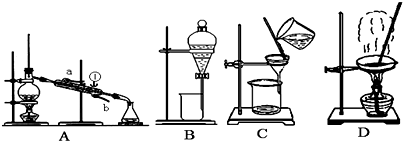
(1)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置______.
(2)从碘水中分离出I2,选择装置______,该分离方法的名称为______.
(3)装置A中①的名称是______,进出水的方向是______.
(4)装置B在分液时为使液体顺利下滴,应进行的具体操作是______.(填代表选项的字母)
A.应该先将分液漏斗上的活塞拿下后再打开旋塞放出液体
B.加热
C.使分液漏斗上的活塞上的凹槽对准分液漏斗上的小孔后再打开旋塞放出液体.
Ⅱ.某同学按下列步骤配制250mL 0.2mol?L-1NaCl溶液,请回答有关问题.
| 实验步骤 | 有关问题 |
| ①计算所需NaCl的质量 | |
| ②称量NaCl固体 | 用托盘天平需要称量NaCl的质量为______g. |
| ③将NaCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施:______. |
| ④将烧杯中溶液转移至250mL容量瓶中 | 为了防止溶液溅出,应采取什么措施:______. |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1-2厘米处应如何操作: ______. |
(2)取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是______.
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需______.
(4)配制NaCl溶液时,下列操作情况会使结果偏高的是______.
A.移液前,容量瓶中有少量蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶瓶颈刻度线
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容.
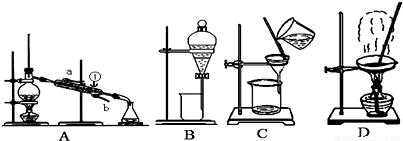
(1)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置______.
(2)从碘水中分离出I2,选择装置______,该分离方法的名称为______.
(3)装置A中①的名称是______,进出水的方向是______.
(4)装置B在分液时为使液体顺利下滴,应进行的具体操作是______.(填代表选项的字母)
A.应该先将分液漏斗上的活塞拿下后再打开旋塞放出液体
B.加热
C.使分液漏斗上的活塞上的凹槽对准分液漏斗上的小孔后再打开旋塞放出液体.
Ⅱ.某同学按下列步骤配制250mL 0.2mol?L-1NaCl溶液,请回答有关问题.
| 实验步骤 | 有关问题 |
| ①计算所需NaCl的质量 | |
| ②称量NaCl固体 | 用托盘天平需要称量NaCl的质量为______g. |
| ③将NaCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施:______. |
| ④将烧杯中溶液转移至250mL容量瓶中 | 为了防止溶液溅出,应采取什么措施:______. |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1-2厘米处应如何操作: ______. |
(2)取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是______.
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需______.
(4)配制NaCl溶液时,下列操作情况会使结果偏高的是______.
A.移液前,容量瓶中有少量蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶瓶颈刻度线
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容.
查看习题详情和答案>>