摘要:(四)化学键
网址:http://m.1010jiajiao.com/timu3_id_192520[举报]
化学键和分子间作用力影响着物质的性质。分子间作用力包括范德华力和氢键。水分子间存在氢键的作用,彼此结合而形成(H2O)n。在冰中每个水分子被4个水分子包围形成变形的正四面体,通过氢键相互连接成庞大的分子晶体——冰。
(1)氢键虽然为分子间作用力的范畴,但氢键具有饱和性和方向性,请你解释氢键的饱和性和方向性:______________________________________________________________。
(2)实验测得冰中氢键的作用能为18.8 kJ·mol-1,而冰的熔化热却为5.0 kJ·mol-1,这说明了____________________________________________。
(3)有机物 的结构可以表示为
的结构可以表示为 (虚线表示氢键),而有机物
(虚线表示氢键),而有机物 只能形成分子间氢键,工业上用水蒸气蒸馏法将A和B进行分离,则首先被蒸出出的成分是__________。
只能形成分子间氢键,工业上用水蒸气蒸馏法将A和B进行分离,则首先被蒸出出的成分是__________。
(4)氨气极易溶于水,除了遵循相似相溶原理外,还有一个重要原因是_______________,NH3·H2O的结构式可以表示为(用虚线表示氢键)___________________________。
化学键和分子间作用力影响着物质的性质。分子间作用力包括范德华力和氢键。水分子间存在氢键的作用,彼此结合而形成(H2O)n。在冰中每个水分子被4个水分子包围形成变形的正四面体,通过氢键相互连接成庞大的分子晶体——冰。
(1)氢键虽然为分子间作用力的范畴,但氢键具有饱和性和方向性,请你解释氢键的饱和性和方向性:______________________________________________________________。
(2)实验测得冰中氢键的作用能为18.8 kJ·mol-1,而冰的熔化热却为5.0 kJ·mol-1,这说明了____________________________________________。
(3)有机物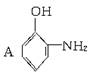 的结构可以表示为
的结构可以表示为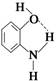 (虚线表示氢键),而有机物
(虚线表示氢键),而有机物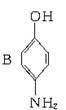 只能形成分子间氢键,工业上用水蒸气蒸馏法将A和B进行分离,则首先被蒸出出的成分是__________。
只能形成分子间氢键,工业上用水蒸气蒸馏法将A和B进行分离,则首先被蒸出出的成分是__________。
(4)氨气极易溶于水,除了遵循相似相溶原理外,还有一个重要原因是_______________,NH3·H2O的结构式可以表示为(用虚线表示氢键)___________________________。
(1)氢键虽然为分子间作用力的范畴,但氢键具有饱和性和方向性,请你解释氢键的饱和性和方向性:______________________________________________________________。
(2)实验测得冰中氢键的作用能为18.8 kJ·mol-1,而冰的熔化热却为5.0 kJ·mol-1,这说明了____________________________________________。
(3)有机物
 的结构可以表示为
的结构可以表示为 (虚线表示氢键),而有机物
(虚线表示氢键),而有机物 只能形成分子间氢键,工业上用水蒸气蒸馏法将A和B进行分离,则首先被蒸出出的成分是__________。
只能形成分子间氢键,工业上用水蒸气蒸馏法将A和B进行分离,则首先被蒸出出的成分是__________。(4)氨气极易溶于水,除了遵循相似相溶原理外,还有一个重要原因是_______________,NH3·H2O的结构式可以表示为(用虚线表示氢键)___________________________。
[化学选修-物质结构与性质]
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为
(2)A最简单的氢化物的分子空间构型是
(3)F和M(质子数为25)两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是
(4)晶体熔点:DC
(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因
查看习题详情和答案>>
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为
C<O<N
C<O<N
.(2)A最简单的氢化物的分子空间构型是
正四面体
正四面体
,其中心原子采取sp3
sp3
杂化,属于非极性分子
非极性分子
(填“极性分子”和“非极性分子”).(3)F和M(质子数为25)两元素的部分电离能数据列于下表:
| 元 素 | M | F | |
| 电离能 (kJ?mol-1) |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
Mn2+的3d轨道电子排布为半满状态较稳定
Mn2+的3d轨道电子排布为半满状态较稳定
;(4)晶体熔点:DC
>
>
EC(填“<、=、>”),原因是MgO与CaO都为离子晶体,Mg2+半径小于Ca2+,则MgO的晶格能大于CaO,所以熔点高
MgO与CaO都为离子晶体,Mg2+半径小于Ca2+,则MgO的晶格能大于CaO,所以熔点高
.(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
H2O2分子间存在氢键,与水分子可形成氢键
H2O2分子间存在氢键,与水分子可形成氢键
?[化学--选修物质结构与性质]
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出F原子的电子排布式
(2)A、B、C的第一电离能由小到大的顺序为
(3)F和M(质子数为25)两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是
(4)已知F晶体的堆积方式与金属钾相同,则F晶胞中F原子的配位数为
(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因
查看习题详情和答案>>
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子M层3d轨道电子为半满状态.请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出F原子的电子排布式
1s22s22p63s23p63d64s2
1s22s22p63s23p63d64s2
,F位于周期表d
d
区.(2)A、B、C的第一电离能由小到大的顺序为
N>O>C
N>O>C
.(3)F和M(质子数为25)两元素的部分电离能数据列于下表:
| 元 素 | M | F | |
| 电能 (kJ?mol-1) |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
Mn2+的3d轨道电子排布为半满状态较稳定
Mn2+的3d轨道电子排布为半满状态较稳定
、而Fe2+的3d轨道电子数为6,不是较稳定状态
而Fe2+的3d轨道电子数为6,不是较稳定状态
;(4)已知F晶体的堆积方式与金属钾相同,则F晶胞中F原子的配位数为
8
8
,一个晶胞中F原子的数目为2
2
.(5)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
氧元素电负性很强,H2O2分子间存在氢键,所以熔沸点比H2S高,H2O2分子与水分子可形成氢键,所以与任意比互溶
氧元素电负性很强,H2O2分子间存在氢键,所以熔沸点比H2S高,H2O2分子与水分子可形成氢键,所以与任意比互溶
.[化学-物质结构与性质]
A、B、C、D、E、F六种元素,A、B、C属于第四周期且单质均为固体.原子处于基态时,A、B原子核外电子均成对,且核电荷数A>B;C与A在周期表属于同一区的元素.如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E、F的原子均有三个能层,E原子的第一电离能至第四电离能(kJ/mol)分别为:
578,1817、2745、11575;E与F能形成原子数目比为1:3,熔点为190℃的化合物Q.请回答:
(1)写出A的基态核外电子排布式
(2)C2+和A2+都能与NH3、H2O等形成配位数为4的配合物.[A(NH3)4]2+和[C(NH3)4]2+都具有对称的空间构型,[C(NH3)4]2+中的两个NH3被两个Cl-取代能得到两种不同结构的产物,而[A(NH3)4]2+中的两个NH3被两个Cl-取代只能得到一种产物,则[C(NH3)4]2+的空间构型为
(3)1mol D的单质分子中存在
(4)实验测得气态无水Q在1.01ⅹ105Pa,t1℃的密度为5.00g/L,气体摩尔体积为53.4L/mol,则此时Q的组成为(写化学式)
查看习题详情和答案>>
A、B、C、D、E、F六种元素,A、B、C属于第四周期且单质均为固体.原子处于基态时,A、B原子核外电子均成对,且核电荷数A>B;C与A在周期表属于同一区的元素.如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E、F的原子均有三个能层,E原子的第一电离能至第四电离能(kJ/mol)分别为:

578,1817、2745、11575;E与F能形成原子数目比为1:3,熔点为190℃的化合物Q.请回答:
(1)写出A的基态核外电子排布式
1s22s22p63s23p63d104s2
1s22s22p63s23p63d104s2
;用最简式表示B、C合金的组成CaCu5
CaCu5
用元素符号表示)(2)C2+和A2+都能与NH3、H2O等形成配位数为4的配合物.[A(NH3)4]2+和[C(NH3)4]2+都具有对称的空间构型,[C(NH3)4]2+中的两个NH3被两个Cl-取代能得到两种不同结构的产物,而[A(NH3)4]2+中的两个NH3被两个Cl-取代只能得到一种产物,则[C(NH3)4]2+的空间构型为
平面正方形
平面正方形
.[A(NH3)4]2+中A的杂化方式为sp3
sp3
.(3)1mol D的单质分子中存在
NA
NA
个σ键NA个
NA个
π键.D的气态氢化物很容易与H+结合,C原子与H+间形成的键叫配位键
配位键
.(4)实验测得气态无水Q在1.01ⅹ105Pa,t1℃的密度为5.00g/L,气体摩尔体积为53.4L/mol,则此时Q的组成为(写化学式)
Al2Cl6
Al2Cl6
,Q属于分子
分子
晶体.