摘要:4. 氨的化学性质 (1)氨与水反应 氨溶于水时.大部分NH3与H2O结合.形成NH3•H2O.NH3•H2O可以部分电离生成 和 .所以氨水显碱性.它能使酚酞试液变红.请写出有关方程式: . (2)氨与酸反应 [实验2] ①实验步骤: , ②观察到的现象: , ③实验结论:挥发性的强酸与氨气在空气中相遇便产生 的现象.如HCl.HBr.HI.HNO3等遇氨气均有该现象产生.而H2SO4.H3PO4无此现象. (3)氨的还原性 工业上利用氨在催化剂存在的情况下跟氧气反应来制取硝酸.写出有关化学方程式.并指出反应的氧化剂.还原剂.
网址:http://m.1010jiajiao.com/timu3_id_192497[举报]
化学可以帮助人类认识改造周围的世界,促进社会发展.
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质.下表为某品牌燕麦片标签中的一部分.
①燕麦片的营养成分中能与水反应生成氨基酸的营养物质是
②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失.因此,烹调富含维生素C的食物时,应该注意
(2)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等.用灼烧法可初步鉴别三种纤维,给三种纤维编号后,分别灼烧产生的气味如下:
则羊毛、棉花的编号分别为
查看习题详情和答案>>
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质.下表为某品牌燕麦片标签中的一部分.
| 每100g含有 营养成分 |
糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 8.1mg |
蛋白质
蛋白质
;每克营养物质氧化时放出能量最多的是油脂
油脂
;人体必需的微量元素是锌
锌
.②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失.因此,烹调富含维生素C的食物时,应该注意
不要高温加热
不要高温加热
;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点食醋
食醋
.(2)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等.用灼烧法可初步鉴别三种纤维,给三种纤维编号后,分别灼烧产生的气味如下:
| 纤维编号 | 1 | 2 | 3 |
| 灼烧时的气味 | 特殊气味 | 烧纸气味 | 烧焦羽毛气味 |
③②
③②
. 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:(1)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是
B
B
(填”A”或”B”).设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2.则m1<
<
m2.(选填”<“、”=“或”>“)(2)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).该反应的平衡常数表达式K=
| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
减小
减小
(填”增大”“减小”或”不变”).在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=| 2nB |
| 3tB |
| 2nB |
| 3tB |
(3)难溶电解质在水溶液中存在着溶解平衡.在某温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数.例如:Mg(OH)2(s)?Mg2+ (aq)+2OH- (aq),某温度下Ksp=c(Mg2+)[c(OH-)]2=2×10-11.若该温度下某MgSO4溶液里c(Mg2+)=0.002mol?L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于
10
10
;该温度下,在0.20L的0.002mol?L-1MgSO4溶液中加入等体积的0.10mol?L-1的氨水溶液,该温度下电离常数K(NH3?H2O)=2×10-5,经计算有
有
(填”有”或”无”)Mg(OH)2沉淀生成.(4)常温下,向某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,则该溶液呈
碱
碱
性.在分析该溶液遇酚酞呈红色的原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中Na2CO3电离出的C| O | 2- 3 |
[化学-物质结构与性质]
铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
(1)基态铬原子的价电子排布式为 .
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂.制备CrO2Cl2的反应为:K2 Cr2O2+3CCl4 2KC+2CrO2Cl2+3COCl2↑.
①上述反应式中非金属元素电负性由大到小的顺序是 (用元素符号表示).
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于 晶体.
③COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为 .
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2nm和7.8×10-2nm.则熔点:NiO FeO(填”<”、“=”或“>”).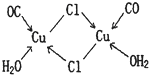
(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2?2H2O],其结构如图.下列说法不正确的是 .(填标号)
A.该复合物中存在化学健类型只有离子键、配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体
D.CO与N2的价电子总数相同,其结构为C≡O
(5)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子.已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 .
查看习题详情和答案>>
铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
(1)基态铬原子的价电子排布式为
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂.制备CrO2Cl2的反应为:K2 Cr2O2+3CCl4 2KC+2CrO2Cl2+3COCl2↑.
①上述反应式中非金属元素电负性由大到小的顺序是
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于
③COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2nm和7.8×10-2nm.则熔点:NiO

(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2?2H2O],其结构如图.下列说法不正确的是
A.该复合物中存在化学健类型只有离子键、配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体
D.CO与N2的价电子总数相同,其结构为C≡O
(5)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子.已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
[化学选考----有机化学]
有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有 (选填序号)。
①加成反应 ②酯化反应 ③加聚反应 ④氧化反应
(2)B分子所含官能团的名称是 、 。
(3)B分子中没有支链,其结构简式是 ,B的具有相同官能团的同分异构体的![]() 结构简式是 。
结构简式是 。
(4)由B制取A的化学方程式是 。
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
![]()
天门冬氨酸的结构简式是 。
查看习题详情和答案>>(16分)化学实验是科学探究的基础。请回答有关实验问题:
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是 :
(2)要检验上面B装置氨气已集满的操作是 则试管已集满。
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如右表:
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光 | |
| 常温气体 | -59-11℃红黄色液体 | 生成亚氯酸盐和氯酸盐 | 爆炸 |
②工业用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图B所示装置模拟工业制法制取并收集液态ClO2,请模仿下图B的装置图和图例,在答题卡的相应图中补充完善装置图,并作必要的标注。
 查看习题详情和答案>>
查看习题详情和答案>>