摘要:随堂练习:
网址:http://m.1010jiajiao.com/timu3_id_192311[举报]
 KMnO4的氧化性随pH的减小而增大.其在酸性介质中还原产物是Mn2+;在中性或碱性介质中还原产物主要是MnO2.
KMnO4的氧化性随pH的减小而增大.其在酸性介质中还原产物是Mn2+;在中性或碱性介质中还原产物主要是MnO2.(1)应该在
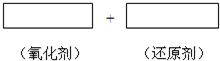
(2)在亚硫酸溶液中滴入酸性KMnO4溶液.将该反应的氧化剂、还原剂和配平后的系数填入正确位置,并标出电子转移的方向和数目
(3)三氯乙烯(C2HCl3)是地下水有机污染物的主要成分,研究显示在地下水中加入KMnO4溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出反应的化学方程式
(4)加入过量的KMnO4才能将水中的三氯乙烯彻底除去.已知n(KMnO4):n(C2HCl3)=5:1时,水样中的三氯乙烯基本完全去除.某地下水样品中三氯乙烯的质量浓度为1×10-4g/L,计算每处理1m3该地下水,需KMnO4
已知反应FeO(s)+C(s)=CO(g)+Fe(s)的△H为正.△S为正(假定△H.△S不随温度而变化),下列叙述中正确的是( )
| A、高温下为自发过程,低温下为非自发过程 | B、低温下为自发过程,高温下为非自发过程 | C、任何温度下均为非自发过程 | D、任何温度下均为自发过程 |
某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c、d表示止水夹).
(1)B是一种可以随开随制,随关随停的制备气体的装置.检验装置B的气密性方法 是 .
(2)上述 (填写序号)相连后的装置可用于制取和收集氯气.写出实验室制取氯气的化学方程式 .
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁的操作是 .
②试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满溶液,则NO2与通入O2的物质的量比为 .
查看习题详情和答案>>

(1)B是一种可以随开随制,随关随停的制备气体的装置.检验装置B的气密性方法 是
(2)上述
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹
②试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满溶液,则NO2与通入O2的物质的量比为
下列对递变规律的描述正确的是( )
| A、氧化性:Na+<K+<Rb+<Cs+ | B、卤素氢化物的稳定性随核电荷数的递增依次增强 | C、在卤素的氢化物中,HI的还原性最强 | D、碱金属元素随核电荷数的递增,熔沸点依次升高 |
(1)二氧化硫是大气污染物之一,空气中的二氧化硫随雨水下降形成酸雨.某校研究性学习小组利用亚硫酸钠固体与硫酸反应(Na2SO3+H2SO4
Na2SO4+SO2↑+H2O)模拟酸雨的形成并验证二氧化硫的部分性质.装置示意图如下,请回答:
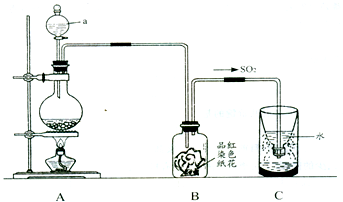
①指出图中仪器a的名称: .
②B装置中淡红色纸花的颜色逐渐褪去,说明SO2有 性.
③反应结束后取出C装置中少量液体,滴加紫色石蕊试液后变 色.
④实验完毕后,为了使多余的二氧化硫被充分吸收,C装置应作如何改进?(用文字说明) .
(2)查阅资料可知:亚硫酸钠遇空气中的氧气或接触某些氧化剂都会生成硫酸钠;亚硫酸钡
是难溶于水,易溶于酸的白色固体,为证实上述亚硫酸钠已有部分变质,两个小组分别设计方案如下:
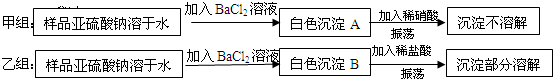
你认为 组的方案得出的结论正确,另一组方案存在的问题是 ;
两组所得到的白色沉淀A、B成分相同,请写出化学式: .
查看习题详情和答案>>
| ||

①指出图中仪器a的名称:
②B装置中淡红色纸花的颜色逐渐褪去,说明SO2有
③反应结束后取出C装置中少量液体,滴加紫色石蕊试液后变
④实验完毕后,为了使多余的二氧化硫被充分吸收,C装置应作如何改进?(用文字说明)
(2)查阅资料可知:亚硫酸钠遇空气中的氧气或接触某些氧化剂都会生成硫酸钠;亚硫酸钡
是难溶于水,易溶于酸的白色固体,为证实上述亚硫酸钠已有部分变质,两个小组分别设计方案如下:

你认为
两组所得到的白色沉淀A、B成分相同,请写出化学式: