摘要:可逆反应和不可逆反应: (1)可逆反应:在同一条件下.能同时向正.逆两个方向进行的反应.通常把从左向右 进行的反应称为正反应.把从右向左的反应称为逆反应.如: N2+3H2 2NH3+Q (2)不可逆反应:在同一条件下.不能同时向两个方向进行的反应.可看成正.逆反应的趋势差别很大.反应“一边倒 .正.逆反应是相对的. (3)可逆反应的特点: a.正反应和逆反应之间具有既对立有统一的关系.即正反应和逆反应是两个方向完全相反的不同的化学反应.但他们有同时存在.不可分离.例如:某容器内有SO2和O2合成SO3的化学反应.那么也一定有SO3分解为SO2和O2的化学反应. b.正反应和逆反应的发生性质相同.例如:SO2具有跟O2合成SO3的性质.SO3也有分解生成SO2和O2的性质. c.正反应和逆反应发生的条件相同.例如:SO2和O2合成SO3和SO3分解为SO2和O2的条件都是催化剂.高温.如果对反应体系施加影响化学反应速度率的措施.正反应速率和逆反应速率都会受到影响.例如升高或者降低温度.增大或者减小压强. 2 SO2+O2 2SO3 和2 SO3 2 SO2+O2的反应速率都会发生相应的变化. d.各反应物.生成物同时存在 .方程式两边的物质互为反应物和生成物.任何一种物质的生成率都小于1.任何一种物质的存在量都大于0.但存在量不能无条件的确定. e.事实上.大部分化学反应都是可逆反应.只不过有的可逆性较弱.有的可逆性很强.
网址:http://m.1010jiajiao.com/timu3_id_192243[举报]
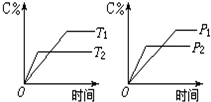 可逆反应mA(s)+nB(g)?pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图(T2>T1),根据图中曲线分析,判断下列叙述中正确的是( )
可逆反应mA(s)+nB(g)?pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图(T2>T1),根据图中曲线分析,判断下列叙述中正确的是( )
查看习题详情和答案>>
可逆反应:2NO2(g)?2NO(g)+O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2;②NO2和NO的物质的量浓度相等;③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态;④混合气体的密度不再改变的状态;⑤混合气体的颜色不再改变的状态.
①单位时间内生成n mol O2的同时生成2n mol NO2;②NO2和NO的物质的量浓度相等;③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态;④混合气体的密度不再改变的状态;⑤混合气体的颜色不再改变的状态.
查看习题详情和答案>>