摘要:下列各组元素都属于短周期金属元素的是 ( ) A.H C N B.Li Na Al C.Mg Al Si D.Na Cl Fe
网址:http://m.1010jiajiao.com/timu3_id_191602[举报]
科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部位于元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成.现有a~g 7种短周期元素,是除氧、硫、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
(1)元素的原子间反应最容易形成离子键的是下列中的
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为
 .
.
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式
查看习题详情和答案>>
| a | |||||||||||||||||
| d | e | ||||||||||||||||
| b | c | f | g | ||||||||||||||
B
B
,元素的原子间反应容易形成共价键的是下列中的C
C
A.c和f B.b和g C.d和g D.d和e(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是
CD
CD
.A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为


(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式
Mg3N2
Mg3N2
,化学键类型为离子键
离子键
,与稀盐酸反应的方程式为Mg3N2+8HCl=3MgCl2+2NH4Cl
Mg3N2+8HCl=3MgCl2+2NH4Cl
.科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部位于元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成.现有a~g 7种短周期元素,是除氧、硫、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
(1)元素的原子间反应最容易形成离子键的是下列中的______,元素的原子间反应容易形成共价键的是下列中的______A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是______.
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为______.
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式______,化学键类型为______,与稀盐酸反应的方程式为______.
查看习题详情和答案>>
| a | |||||||||||||||||
| d | e | ||||||||||||||||
| b | c | f | g | ||||||||||||||
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是______.
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为______.
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式______,化学键类型为______,与稀盐酸反应的方程式为______.
科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部位于元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成.现有a~g 7种短周期元素,是除氧、硫、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
(1)元素的原子间反应最容易形成离子键的是下列中的______,元素的原子间反应容易形成共价键的是下列中的______A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是______.
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为______.
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式______,化学键类型为______,与稀盐酸反应的方程式为______.
查看习题详情和答案>>
| a | |||||||||||||||||
| d | e | ||||||||||||||||
| b | c | f | g | ||||||||||||||
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是______.
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为______.
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式______,化学键类型为______,与稀盐酸反应的方程式为______.
查看习题详情和答案>>
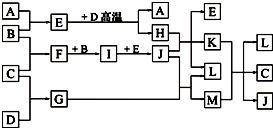 如图,常温下单质A、B为气体,单质C为固体,它们依次分别由短周期元素甲、乙、丙组成,甲元素原子核外电子数等于其电子层数,乙、丙同主族;E常温下为液体,G、H为黑色固体,D是常见金属(反应条件多数略去).
如图,常温下单质A、B为气体,单质C为固体,它们依次分别由短周期元素甲、乙、丙组成,甲元素原子核外电子数等于其电子层数,乙、丙同主族;E常温下为液体,G、H为黑色固体,D是常见金属(反应条件多数略去).回答下列问题:
(1)化合物E的沸点高于化合M的沸点,原因是
(2)甲、乙两种元素可以形成两种化合物,其中一种化合物含有4个原子核,该化合物的结构式为
(3)E与D高温反应的化学方程式为
(4)实验室在保存L溶液时,需加入少量D,理由是
(5)已知一定条件下,每1mol F与单质B完全反应生成I放出热量98.0kJ,若2mol F与1mol B在此条件下发生反应,达平衡时,放出热量为176.4kJ,则F的转化率为
①4mol F、2mol B ②2mol F、2mol B、2mol I
③1mol F、0.5mol B、1mol I ④3mol I、1mol Ne.