网址:http://m.1010jiajiao.com/timu3_id_191435[举报]
【查阅资料】N2的制法有下列三种方案:
方案1:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉.
方案2:加热NaNO2和NH4Cl的浓溶液制得N2.
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2.
【实验准备】以实验室常见仪器(药品)等设计的部分装置如图(有的夹持和加热仪器未画出).
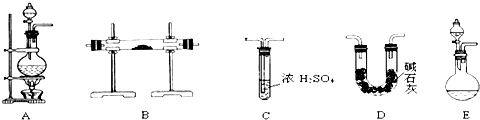
【分析交流】
(1)若按方案1制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的顺序连接的顺序是(填写序号,下同)
(2)若以排水法收集N2,其中会混入水蒸气.但也不宜用排空气法,其原因是
(3)若以方案2制得N2,应选择的发生装置是
(4)上述三个方案中,制得的N2纯度最差的是
填写下列空白.
[实验方案]铝镁合金粉末
| NaOH溶液 |
[实验步骤]
步骤1:称取5.4g铝镁合金粉末样品,投入VmL2.0mol?L-1NaOH溶液中,充分反应.
步骤2:过滤、洗涤、干燥、称量固体.
[交流与讨论]
(1)实验中发生反应的化学方程式是
(2)参与反应的NaOH溶液的体积V≥
(3)步骤2中,如果经两次过滤滤液仍浑浊,则原因可能是
(4)步骤2中,若未洗涤固体,测得镁的质量分数将
[实验拓展]请你另设计-个实验方案(用上述方案的试剂),测定该铝镁合金中镁的质量分数.
要求:从图中挑选所需的仪器,画出该方案的实验装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置不用画),并标明所用试剂.
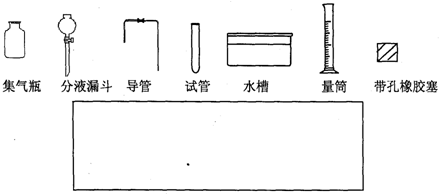
铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计以下实验方案进行探究。填写下列空白。
[实验方案] 铝镁合金粉末![]() 测定剩余固体质量
测定剩余固体质量
[实验步骤]
步骤1:称取5.4g铝镁合金粉末样品,投入VmL 2.0mol·L—1NaOH溶液中,充分反应。
步骤2:过滤、洗涤、干燥、称量固体。
[交流与讨论]
(1) 实验中发生反应的化学方程式是 ;
(2)参与反应的NaOH溶液的体积V≥ ;
(3)步骤2中,如果经两次过滤滤液仍浑浊,则原因可能是_________(只填一点);
(4)步骤2中,若未洗涤固体,测得镁的质量分数将 (填“偏高”或“偏低”)。
[实验拓展] 请你另设计一个实验方案(用上述方案的试剂),测定该铝镁合金中镁的质量分数。
要求:从下图中挑选所需的仪器,画出该方案的实验装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置不用画),并标明所用试剂.


(12分) Ⅰ.下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。

(1)图中属于烷烃的是 (填编号)属于烯烃的是 ,(填编号)
(2)上图中与B互为同分异构体但不属于同种类的物质的是: 。(填编号)
Ⅱ.课本“交流•研讨”栏目有这样一组数据:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收249kJ的能量;形成水分子中1 mol H—O键能够释放463kJ能量。
下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在下边的横线上。

① kJ ② kJ ③ kJ
查看习题详情和答案>>
I.下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。
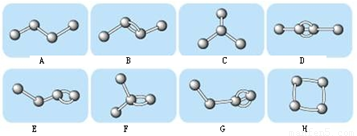
(1)图中属于烷烃的是 (填编号);属于烯烃的是 (填编号);
(2)上图中与B互为同分异构体但不属于同种类的物质的是: 。(填编号)
II.课本“交流•研讨”栏目有这样一组数据:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收249kJ的能量;形成水分子中1 mol H—O键能够释放463kJ能量。
下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在下边的横线上。
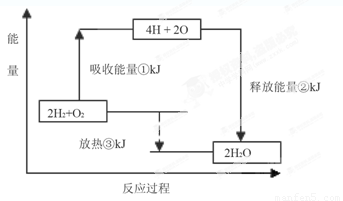
① kJ;② kJ;③ kJ。
查看习题详情和答案>>