摘要:有Mg和Al的混合物7.8g.放入稀盐酸中产生气体8.96L.求该混合物中Mg和Al的物质的量各是多少? 期末复习练习四答案
网址:http://m.1010jiajiao.com/timu3_id_190858[举报]
现有等物质的量的Mg和Al的混合物a g与100ml盐酸反应,(气体体积均以标准状况计算)
(1)该混合物中Mg和Al的质量比为
(2)如果金属与盐酸恰好完全反应,则盐酸的浓度为
mol/L
mol/L
(3)如果反应后金属有剩余,盐酸不足,要计算生成H2的体积,还需要知道
(4)如盐酸过量,生成H2的体积为
L
LL
(5)若Mg和Al不是以等物质的量混合,则a g混合物与足量盐酸完全反应时生成H2体积(V)的范围是
L<V(H2)<
L
L<V(H2)<
L.
查看习题详情和答案>>
(1)该混合物中Mg和Al的质量比为
8:9
8:9
(2)如果金属与盐酸恰好完全反应,则盐酸的浓度为
| 50a |
| 51 |
| 50a |
| 51 |
(3)如果反应后金属有剩余,盐酸不足,要计算生成H2的体积,还需要知道
盐酸的物质的量浓度
盐酸的物质的量浓度
(4)如盐酸过量,生成H2的体积为
| 56a |
| 51 |
| 56a |
| 51 |
(5)若Mg和Al不是以等物质的量混合,则a g混合物与足量盐酸完全反应时生成H2体积(V)的范围是
| 22.4a |
| 24 |
| 22.4a |
| 18 |
| 22.4a |
| 24 |
| 22.4a |
| 18 |
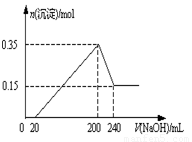
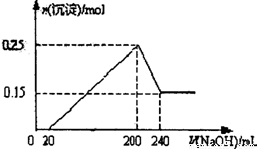
将一定质量的Mg和Al的混合物投入2.0mol/L,250 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示。则下列说法正确的是( )

A.当加氢氧化钠溶液体积为20mL时,溶液的pH值等于7
B.当加氢氧化钠溶液体积为20mL时,溶液中的溶质只有硫酸镁和硫酸铝
C.NaOH溶液的物质的量浓度为5 mol/L
D.生成的H2在标准状况下的体积为11.2 L
查看习题详情和答案>>
现有等物质的量的Mg和Al的混合物a g与100 ml盐酸反应,(气体体积均以标准状况计算)
(1)、该混合物中Mg和Al的质量比为
(2)、如果金属与盐酸恰好完全反应,则盐酸的浓度为
(3)、如果反应后金属有剩余,盐酸不足,要计算生成H2的体积,还需要知道