网址:http://m.1010jiajiao.com/timu3_id_190774[举报]
(12分)
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
回答下列问题:
(1)上述方案中,能测出Mg的质量分数的方案是 (填写代号,下同)
A.实验设计1 B.实验设计2 C.实验设计3 D.都可以
(2)上述方案中的化学反应体现了Mg、Al的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)某同学设计了右图装置。该装置适合的实验设计是
A.实验设计1 B.实验设计2 C.实验设计3
用该装置测定镁铝合金中镁的质量分数,所需的实验操作是
。
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.称量反应前后,装置和药品的总质量
(4)若按实验设计3进行实验。将m g镁铝合金,溶于过量盐酸中,再加入过量的NaOH溶液,可得到白色沉淀,该沉淀物质是 (填化学式);将此沉淀洗净、干燥后,称得质量为w g。求合金中镁的质量分数 ;
查看习题详情和答案>>
(12分)
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:

回答下列问题:
(1)上述方案中,能测出Mg的质量分数的方案是 (填写代号,下同)
A.实验设计1 B.实验设计2 C.实验设计3 D.都可以
(2)上述方案中的化学反应体现了Mg、Al的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)某同学设计了右图装置。该装置适合的实验设计是

A.实验设计1 B.实验设计2 C.实验设计3
用该装置测定镁铝合金中镁的质量分数,所需的实验操作是
。
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.称量反应前后,装置和药品的总质量
(4)若按实验设计3进行实验。将m g镁铝合金,溶于过量盐酸中,再加入过量的NaOH溶液,可得到白色沉淀,该沉淀物质是 (填化学式);将此沉淀洗净、干燥后,称得质量为w g。求合金中镁的质量分数 ;
查看习题详情和答案>>
钛被认为是21世纪的重要金属材料.纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用.
Ⅰ.目前大规模生产钛的方法是:
第一步 首先将金红石(TiO2)、炭粉混合,在高温条件下通入氯气制得TiCl4;
第二步 在氮气氛围中用过量的镁在加热条件下与TiCl4反应制得金属钛.
已知:①C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g)
ΔH=-566 kJ·mol-1③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141 kJ·mol-1
则
:TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=________.Ⅱ.
纳米TiO2可通过TiCl4水解制备,过程为:在冰水浴强力搅拌下,将一定量的TiCl4滴加到溶有HCl和(NH4)2SO4的冰的TiCl4水溶液中,控制TiCl4浓度为1.1 mol/L时撤去冰浴,逐步升温到95℃,恒温水解1h后,滴加氨水,调节溶液pH约为6,自然冷却后过滤,产物经水洗至无Cl-和SO42-后,再用乙醇洗涤3遍,高温煅烧2h制备纳米TiO2.(1) TiCl4水解生成TiO2·x H2O的化学方程式为________.
(2)简述升温和调节溶液pH的目的:________.
Ⅲ.在制造TiO2过程中,需要测定Ti(Ⅳ)的含量.测定时首先将TiO2溶解为钛液,然后取10 mL用水冲稀10倍,加过量铝粉,充分振荡,使其完全反应:
Ti(Ⅳ)+Al→Ti3++Al3+.过滤后,取出滤液20 mL,向其中滴加2~3滴KSCN溶液,再加5 mL蒸馏水振荡,用酸式滴定管滴加0.1 mol/L FeCl3溶液,终点到来时,用去了30 mL的FeCl3溶液.
(1)滴定终点的现象是________.
(2)原钛液的物质的量浓度为________.
(3)若在滴定终点读取滴定管刻度时,俯视标准液液面,则使Ti(Ⅳ)的含量测定结果________(填“偏高”、“偏低”或“无影响”).
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为 g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:镁铝合金 充分反应后测定剩余固体质量
充分反应后测定剩余固体质量 g
g
实验设计2:镁铝合金 生成的气体在标准状况下的体积为VL。
生成的气体在标准状况下的体积为VL。
请回答以下问题:
实验设计1:
(1)镁的质量分数: 。
(2)在溶解、过滤中使用的玻璃仪器有 __________ 。
(3)过滤后洗涤沉淀的操作方法是________________________________________
____________________________________________________。
(4)如果过滤得到沉淀没有用蒸馏水洗涤数次后,烘干,再测定剩余固体质量。测得镁的质量分数量会 (填“偏大”、“偏小”或“无影响”)。
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为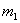 g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:镁铝合金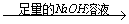 充分反应后测定剩余固体质量
充分反应后测定剩余固体质量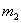 g
g
实验设计2:镁铝合金 生成的气体在标准状况下的体积为VL。
生成的气体在标准状况下的体积为VL。
请回答以下问题:
实验设计1:
(1)镁的质量分数: 。
(2)在溶解、过滤中使用的玻璃仪器有 __________ 。
(3)过滤后洗涤沉淀的操作方法是________________________________________
____________________________________________________。
(4)如果过滤得到沉淀没有用蒸馏水洗涤数次后,烘干,再测定剩余固体质量。测得镁的质量分数量会 (填“偏大”、“偏小”或“无影响”)。
查看习题详情和答案>>