摘要:Cl2的实验室制取与性质验证是高中化学实验的基础实验之一.结合所给装置图Ⅰ.Ⅱ.Ⅲ.回答下列问题. ⑴在制取有毒气体时.通常使用“制备→净化→干燥→收集→尾气处理 五部分装置.在图Ⅰ中E.F属于尾气处理装置.其中E的作用是 . ⑵写出图Ⅰ圆底烧瓶中发生反应的化学方程式 ,在F所指的装置中.通常盛放的试剂为 .写出该装置中发生的离子反应方程式 . ⑶请你结合图Ⅱ.描述该实验的实验现象 . ⑷将装有饱和氯水的烧瓶.倒置于水槽中.放置在阳光直射处.如图Ⅲ所示.一段时间后.可以观察有气泡产生.该反应的化学方程式为 . ⑸用高锰酸钾和浓盐酸在室温下就能很快制得氯气.由此可以比较二氧化锰和高锰酸钾中氧化性较强的是 .
网址:http://m.1010jiajiao.com/timu3_id_189240[举报]
Cl2的实验室制取与性质验证是高中化学实验的基础实验之一,结合所给装置图Ⅰ、Ⅱ、Ⅲ,回答下列问题.
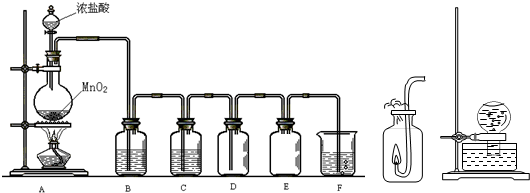
(1)在制取有毒气体时,通常使用“制备→净化→干燥→收集→尾气处理”五部分装置.在图Ⅰ中E、F属于尾气处理装置,其中E的作用是 .
(2)写出图Ⅰ圆底烧瓶中发生反应的化学方程式 ;在F所指的装置中,通常盛放的试剂为 ,写出该装置中发生的离子反应方程式 .
(3)请你结合图Ⅱ,描述该实验的实验现象 .
(4)将装有饱和氯水的烧瓶,倒置于水槽中,放置在阳光直射处,如图Ⅲ所示.一段时间后,可以观察有气泡产生,该反应的化学方程式为 .
(5)用高锰酸钾和浓盐酸在室温下就能很快制得氯气,由此可以比较二氧化锰和高锰酸钾中氧化性较强的是 .
查看习题详情和答案>>

(1)在制取有毒气体时,通常使用“制备→净化→干燥→收集→尾气处理”五部分装置.在图Ⅰ中E、F属于尾气处理装置,其中E的作用是
(2)写出图Ⅰ圆底烧瓶中发生反应的化学方程式
(3)请你结合图Ⅱ,描述该实验的实验现象
(4)将装有饱和氯水的烧瓶,倒置于水槽中,放置在阳光直射处,如图Ⅲ所示.一段时间后,可以观察有气泡产生,该反应的化学方程式为
(5)用高锰酸钾和浓盐酸在室温下就能很快制得氯气,由此可以比较二氧化锰和高锰酸钾中氧化性较强的是
Cl2的实验室制取与性质验证是高中化学实验的基础实验之一,结合所给装置图Ⅰ、Ⅱ、Ⅲ,回答下列问题.
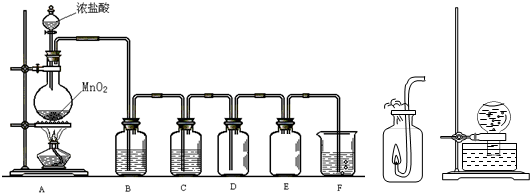
(1)在制取有毒气体时,通常使用“制备→净化→干燥→收集→尾气处理”五部分装置.在图Ⅰ中E、F属于尾气处理装置,其中E的作用是______.
(2)写出图Ⅰ圆底烧瓶中发生反应的化学方程式______;在F所指的装置中,通常盛放的试剂为______,写出该装置中发生的离子反应方程式______.
(3)请你结合图Ⅱ,描述该实验的实验现象______.
(4)将装有饱和氯水的烧瓶,倒置于水槽中,放置在阳光直射处,如图Ⅲ所示.一段时间后,可以观察有气泡产生,该反应的化学方程式为______.
(5)用高锰酸钾和浓盐酸在室温下就能很快制得氯气,由此可以比较二氧化锰和高锰酸钾中氧化性较强的是______.
查看习题详情和答案>>

(1)在制取有毒气体时,通常使用“制备→净化→干燥→收集→尾气处理”五部分装置.在图Ⅰ中E、F属于尾气处理装置,其中E的作用是______.
(2)写出图Ⅰ圆底烧瓶中发生反应的化学方程式______;在F所指的装置中,通常盛放的试剂为______,写出该装置中发生的离子反应方程式______.
(3)请你结合图Ⅱ,描述该实验的实验现象______.
(4)将装有饱和氯水的烧瓶,倒置于水槽中,放置在阳光直射处,如图Ⅲ所示.一段时间后,可以观察有气泡产生,该反应的化学方程式为______.
(5)用高锰酸钾和浓盐酸在室温下就能很快制得氯气,由此可以比较二氧化锰和高锰酸钾中氧化性较强的是______.
在实验室中用下列装置进行有关实验探究.请回答下列问题:
Ⅰ.气体制备时需检查装置的气密性,如下图所示各装置,肯定不符合气密性检查要求的是______.

Ⅱ.若用下列装置③制取并收集干燥的NH3,烧瓶内装的试剂是______.收集装置应选择
______(填装置序号).证明氨气已收集满的操作是______.

Ⅲ.二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品.
②有关物质的部分性质如下表:
设计实验装置图如下:
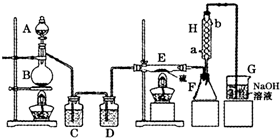
(1)B中反应的离子方程式:______;
(2)H中冷水的方向为______进______出.
(3)为了提高S2Cl2的纯度,关键的操作是控制好温度和______.
(4)尾气处理装置存在明显的缺陷,如何改正:______.
查看习题详情和答案>>
Ⅰ.气体制备时需检查装置的气密性,如下图所示各装置,肯定不符合气密性检查要求的是______.

Ⅱ.若用下列装置③制取并收集干燥的NH3,烧瓶内装的试剂是______.收集装置应选择
______(填装置序号).证明氨气已收集满的操作是______.

Ⅲ.二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品.
②有关物质的部分性质如下表:
| 物质 | 熔点/℃ | 沸点℃ | 化学性质 | ||||
| S | 112.8 | 444.6 | 略 | ||||
| S2Cl2 | -77 | 137 | 遇水生成HCl,SO2,S;300℃以上完全分解; S2Cl2+Cl2
|

(1)B中反应的离子方程式:______;
(2)H中冷水的方向为______进______出.
(3)为了提高S2Cl2的纯度,关键的操作是控制好温度和______.
(4)尾气处理装置存在明显的缺陷,如何改正:______.
1774年瑞典化学家舍勒用软锰矿(主要成分是二氧化锰)和浓盐酸共热得到黄绿色气体。甲、乙两个同学分别采取上述反应原理,各制取一瓶氯气,并用其验证Cl2与水反应产物的性质。甲、乙同学采用的装置如图所示。回答下列问题
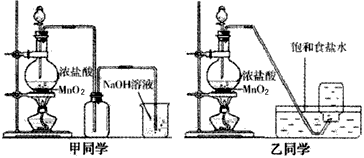
(1)写出实验中制备氯气的化学方程式____________________
(2)对于乙同学的实验装备,要停止实验,其操作顺序是___________。
①停止加热②取出集气瓶盖好③将导管伸入到烧碱溶液中
(3)甲、乙两同学分别向收集到的氯气中加入适量的水,充分振荡后分成两份,均做验证氯气与水反应所得产物性质的实验。实验操作、现象、结论记录如下
(2)对于乙同学的实验装备,要停止实验,其操作顺序是___________。
①停止加热②取出集气瓶盖好③将导管伸入到烧碱溶液中
(3)甲、乙两同学分别向收集到的氯气中加入适量的水,充分振荡后分成两份,均做验证氯气与水反应所得产物性质的实验。实验操作、现象、结论记录如下

请你填写下表评价甲、乙同学实验①、②的结论(填合理或不合理)
若不合理,理由是_______________________
(4)丙同学查阅资料发现HClO的氧化性大于MnO2,拟用下列四组试剂在实验室制取氯气
A.CaCl2和次氯酸 B.浓盐酸和NaClO C.浓盐酸和次氯酸 D.固体NaCl固体NaClO和浓硫酸
你认为上述四组试剂中____组试剂符合实际,且Cl的原子利用率又高;写出这个反应的化学方程式
________________________
查看习题详情和答案>>
(4)丙同学查阅资料发现HClO的氧化性大于MnO2,拟用下列四组试剂在实验室制取氯气
A.CaCl2和次氯酸 B.浓盐酸和NaClO C.浓盐酸和次氯酸 D.固体NaCl固体NaClO和浓硫酸
你认为上述四组试剂中____组试剂符合实际,且Cl的原子利用率又高;写出这个反应的化学方程式
________________________
