摘要:X是VIA族元素.以下一些该元素组成的粒子的化学式中的n值不一定为2的是( ) A.阴离子:[ ]n- B.氧化物:XOn C.气态氢化物:HnX D.含氧酸:HnXO4
网址:http://m.1010jiajiao.com/timu3_id_188335[举报]
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题
Ⅰ.(1)请画出元素⑧的离子结构示意图 .
(2)元素⑦中质子数和中子数相等的同位素符号是 .
(3)④、⑤、⑦的原子半径由大到小的顺序为 .
(4)⑦和⑧的最高价氧化物对应水化物的酸性强弱为 > .
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为 .
(6)周期表中,同一主族元素化学性质相似;同时有些元素和它在周期表中左上方或右下方的另一主族元素的化学性质也相似,如Li与Mg,这称为对角线规则.上表中与铍的化学性质相似的元素有(填元素名称) .铍的最高价氧化物对应水化物属于两性化合物,该化合物的化学式是 ,能够说明其具有两性的反应离子方程式为: ; .
Ⅱ.由表中①~⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答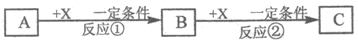
(1)若X是强氧化性单质,则A不可能是 (填序号).
a.S b.N2 c.Na d.Mg e.Al
(2)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属阳离子的化学试剂 ,现象是 ;又知在酸性溶液中该金属阳离子能被双氧水氧化,写出该反应的离子方程式: .
(3)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为 ,写出A与C两溶液反应的离子方程式: .
查看习题详情和答案>>
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素⑦中质子数和中子数相等的同位素符号是
(3)④、⑤、⑦的原子半径由大到小的顺序为
(4)⑦和⑧的最高价氧化物对应水化物的酸性强弱为
(5)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为
(6)周期表中,同一主族元素化学性质相似;同时有些元素和它在周期表中左上方或右下方的另一主族元素的化学性质也相似,如Li与Mg,这称为对角线规则.上表中与铍的化学性质相似的元素有(填元素名称)
Ⅱ.由表中①~⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答

(1)若X是强氧化性单质,则A不可能是
a.S b.N2 c.Na d.Mg e.Al
(2)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属阳离子的化学试剂
(3)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为